Какъв вид лекарство е бетаферон за какво заболяване. Betaferon - инструкции за употреба. Международно непатентно наименование
Лиофилизиран прах за инжекционен разтвор - 1 флакон. интерферон бета-1b - 0,3 mg (съответства на 9,6 милиона IU) помощни вещества: човешки албумин; манитол 1 ml от приготвения разтвор съдържа 0,25 mg (8 милиона IU) рекомбинантен интерферон бета-1b 1 ml воден разтворител за приготвяне на инжекционен разтвор съдържа 5,4 mg натриев хлорид във флакони, заедно с разтворител в спринцовки или флакони със спиртни кърпички или без дъна; в кутия по 5 или 15 комплекта.
Описание на лекарствената форма
Лиофилизат: лиофилизирана бяла маса. Разтворител: бистър разтвор без частици. Приготвен разтвор: леко опалесциращ до опалесциращ разтвор, безцветен или светложълт.
Фармакокинетика
След s / c приложение в препоръчителната доза от 0,25 mg, концентрацията на интерферон бета-1b в кръвта е ниска или изобщо не се открива. След s / c приложение на 0,5 mg Betaferon® на здрави доброволци, Cmax в плазмата е около 40 IU / ml 1-8 часа след инжектирането. В това проучване абсолютната бионаличност на Betaferon®, когато се прилага s / c, е приблизително 50%. При интравенозно приложение клирънсът и T 1/2 на лекарството от серума са средно 30 ml / min / kg и съответно 5 часа. Въвеждането на Betaferon през ден не води до повишаване на нивото на лекарството в кръвната плазма, неговите фармакокинетични параметри също не се променят по време на терапията. При подкожно приложение на Betaferon® в доза от 0,25 mg през ден при здрави доброволци, нивата на маркерите за биологичен отговор (неоптерин, бета2-микроглобулин и имуносупресивния цитокин IL-10) значително се повишават в сравнение с изходните стойности 6 -12 часа след приложението на първите лекарствени дози. Cmax се достига след 40-124 часа и остава повишена през целия 7-дневен (168 часа) период на изследване.
Фармакодинамика
Активното вещество на Betaferon® (интерферон бета-1b) има антивирусно и имунорегулиращо действие. Механизмите на действие на интерферон бета-1b при множествена склероза не са напълно установени. Известно е обаче, че биологичният ефект на интерферон бета-1b се медиира от взаимодействието му със специфични рецептори, открити на повърхността на човешки клетки. Свързването на интерферон бета-1b с тези рецептори индуцира експресията на редица вещества, които се считат за медиатори на биологичните ефекти на интерферон бета-1b. Съдържанието на някои от тези вещества е определено в серума и фракциите на кръвните клетки на пациенти, лекувани с интерферон бета-1b. Интерферон бета-1b намалява капацитета на свързване и експресията на рецепторите за гама-интерферон, засилва тяхното разпадане. В допълнение, интерферон бета-1b повишава супресорната активност на мононуклеарните клетки на периферната кръв.
Клинична фармакология
Както при пристъпно-ремитентна, така и при вторично прогресираща множествена склероза, лечението с Betaferon® намалява честотата (с 30%) и тежестта на клиничните екзацербации на заболяването, броя на хоспитализациите и необходимостта от лечение със стероиди, а също така удължава продължителността на ремисията . При пациенти с вторично прогресираща множествена склероза лечението с Betaferon® позволява да се забави по-нататъшното прогресиране на заболяването и настъпването на инвалидизация, вкл. тежки (т.е. когато пациентите са принудени постоянно да използват инвалидна количка) до 12 месеца. Този ефект се наблюдава при пациенти с и без екзацербации на заболяването, както и с всеки индекс на инвалидност (изследването включва пациенти с резултат от 3,0 до 6,5 точки по разширената скала за инвалидност EDSS). Резултатите от ЯМР на мозъка на пациенти с рецидивираща и вторично прогресираща множествена склероза по време на лечение с Betaferon® потвърждават значителен положителен ефект на лекарството върху тежестта на патологичния процес, както и значително намаляване на образуването на нови активни огнища .
Показания за употреба Betaferon
клинично изолиран синдром (CIS) (единственият клиничен епизод на демиелинизация, предполагащ множествена склероза, при условие че са изключени алтернативни диагнози) с възпалителен процес, достатъчен да изисква интравенозни кортикостероиди за забавяне на прехода към клинично значима множествена склероза (CRMS) при пациенти с висок риск от неговото развитие. Няма общоприето определение за висок риск. Според проучването пациентите с монофокален CIS (клинични прояви на 1 лезия в ЦНС) и >=9 T2 фокуса на MRI и/или фокуси, натрупващи контрастно вещество, са изложени на висок риск от развитие на CRMS. Пациентите с мултифокална CIS (клинични прояви на >1 лезия в ЦНС) са изложени на висок риск от развитие на CRMS, независимо от броя на огнищата при MRI; пристъпно-ремитентна множествена склероза (RRMS) - за намаляване на честотата и тежестта на екзацербациите при амбулаторни пациенти (т.е. пациенти, способни да ходят без помощ) с анамнеза за най-малко 2 екзацербации през последните 2 години, последвани от пълно или непълно възстановяване на неврологичните дефицит; вторично прогресираща множествена склероза с активен ход на заболяването, характеризиращ се с екзацербации или изразено влошаване на неврологичните функции през последните две години - за намаляване на честотата и тежестта на клиничните екзацербации на заболяването, както и за забавяне на скоростта на прогресия на заболяването.
Противопоказания за употребата на Betaferon
свръхчувствителност към естествен или рекомбинантен интерферон бета или човешки албумин в историята; бременност; кърмене. С ВНИМАНИЕ При следните заболявания: сърдечни заболявания, по-специално III-IV стадий на сърдечна недостатъчност (по класификацията на NYHA), кардиомиопатия; депресия и / или суицидни мисли (включително история), епилептични припадъци в историята; моноклонална гамапатия; анемия, тромбоцитопения, левкопения; чернодробна дисфункция; възраст до 18 години (поради липса на достатъчен опит в приложението).
Betaferon Употреба по време на бременност и деца
Противопоказан при бременност. Въпреки това, не е известно дали Betaferon® може да причини увреждане на плода, когато се прилага при бременни жени или да повлияе на човешката репродуктивна функция. При контролирани клинични проучвания при пациенти с множествена склероза има случаи на спонтанен аборт. При проучвания при резус маймуни, човешкият интерферон бета-1b е ембриотоксичен и при по-високи дози предизвиква повишаване на честотата на абортите. Жените в детеродна възраст трябва да използват подходящи контрацептивни методи по време на лечението с това лекарство. В случай на бременност по време на лечение с Betaferon® или планирана бременност, трябва да се препоръча прекъсване на лечението. Не е известно дали интерферон бета-1b се екскретира в кърмата. Като се има предвид възможността за сериозни нежелани реакции при кърмачета, кърменето трябва да се преустанови или лекарството да се преустанови.
Betaferon странични ефекти
По-долу са нежеланите реакции, наблюдавани с честота 2% или по-висока, отколкото в групата на плацебо (неактивно лекарство) при пациенти, които по време на клинични проучвания са получавали Betaferon® в доза от 0,25 mg или 0,16 mg / m2 през ден за до три години. Общи реакции: реакция на мястото на инжектиране, астения (слабост), комплекс от грипоподобни симптоми, главоболие, треска, втрисане, коремна болка, болка в гърдите, болка с различна локализация, общо неразположение, некроза на мястото на инжектиране. Сърдечно-съдова система: периферен оток, вазодилатация, периферно съдово заболяване, хипертония, сърцебиене, тахикардия. Храносмилателна система: гадене, запек, диария, диспепсия. Кръв и лимфна система: лимфоцитопения (= 10%, често - \u003d 1%, понякога - \u003d 0,1%, рядко - \u003d 0,01% и много рядко -
лекарствено взаимодействие
Не са провеждани специални проучвания за взаимодействието на Betaferon® с други лекарства. Ефектът на Betaferon® в доза от 0,25 mg (8 милиона IU) през ден върху лекарствения метаболизъм при пациенти с множествена склероза не е известен. На фона на употребата на Betaferon®, кортикостероидите и ACTH, предписани до 28 дни при лечение на екзацербации, се понасят добре. Употребата на Betaferon® едновременно с други имуномодулатори, в допълнение към кортикостероидите или ACTH, не е проучвана. Интерфероните намаляват активността на чернодробните цитохром Р450-зависими ензими при хора и животни. Трябва да се внимава при предписване в комбинация с лекарства с тесен терапевтичен индекс, чийто клирънс зависи до голяма степен от чернодробната система на цитохром Р450 (например антиепилептици, антидепресанти). Трябва да се внимава при едновременната употреба на всякакви лекарства, които засягат хемопоетичната система.
Дозировка Betaferon
P / c, за един ден. Лечението с Betaferon® трябва да започне под наблюдението на лекар с опит в лечението на множествена склероза. Понастоящем въпросът за продължителността на лечението с Betaferon® остава нерешен. В клинични проучвания продължителността на лечението при пациенти с пристъпно-ремитентна и вторично прогресираща множествена склероза е достигнала съответно 5 и 3 години. Продължителността на курса се определя от лекаря. Приготвяне на инжекционния разтвор A. Опаковка на лекарството, съдържаща флакони и предварително напълнени спринцовки: Използвайте предоставената готова спринцовка с разтворител и игла, за да разтворите лиофилизирания прах от интерферон бета-lb за инжектиране. Б. Опаковка с лекарства, съдържаща флакони, предварително напълнени спринцовки, адаптер за флакон с игла и тампони със спирт: Използвайте предоставените предварително опаковани спринцовка с разредител и адаптер за флакон с игла, за да разтворите лиофилизирания бета-lb интерферон на прах за инжектиране. 1,2 ml разтворител (0,54% разтвор на натриев хлорид) се инжектира в бутилка с Betaferon®. Прахът трябва да се разтвори напълно, без да се разклаща. Преди употреба готовият разтвор трябва да се провери, при наличие на частици или промяна в цвета на разтвора не трябва да се използва. 1 ml от приготвения разтвор съдържа препоръчителната доза Betaferon® - 0,25 mg (8 милиона IU). Ако инжекцията не е приложена в определеното време, тогава е необходимо лекарството да се приложи възможно най-скоро. Следващата инжекция се прави след 48 часа.
Предозиране
При въвеждането на Betaferon® интравенозно в доза до 5,5 mg (176 милиона IU) 3 пъти седмично при възрастни пациенти с рак не са открити сериозни нежелани реакции.
Сега можете да закупите "Betaferon" чрез интернет на изгодна цена и да поръчате доставката му в Москва или региона. За регистрираните потребители на аптека Бурденко цената на лекарствата е по-ниска, отстъпката за Betaferon ще бъде 2-5%. Цената на доставката на лекарства в Русия ще бъде уточнена от нашия мениджър.
Описание на лекарството "Betaferon"
Активното вещество на лекарството "Betaferon" е интерферон бета-1b. Проявява антивирусна и имунорегулираща активност. Лекарството причинява намаляване на капацитета на свързване и експресията на рецепторите за гама-интерферон, увеличава тяхното разпадане. Насърчава повишаването на супресорната активност на мононуклеарните клетки в периферната кръв.
Механизмът на терапевтичния ефект на Betaferon при пациенти с множествена склероза не е установен със сигурност. Известно е обаче, че биологичният ефект на неговата активна съставка се медиира от взаимодействие със специфични рецептори на клетъчната повърхност. Това предизвиква експресията на редица вещества, считани за медиатори на биоефектите на интерферон бета-1b.
Начин на приложение
Лекарството се предписва s / c, главно през ден.
"Betaferon" трябва да се приема под наблюдението на лекар с опит в лечението на множествена склероза, следователно, преди да купите лекарството "Betaferon", консултирайте се със специалист.
Дозов режим
Продължителността на лечението с Betaferon се определя от лекуващия лекар. Еднократната доза, препоръчана според инструкциите, е 250 mcg или 8 милиона IU. В случай на случайно пропускане на инжекция, лекарството трябва да се приложи възможно най-скоро. Следващият път, когато лекарството трябва да се приложи след 48 часа.
Показания за употреба на Betaferon
- CIS (клинично изолиран синдром);
- активна множествена склероза, вторично прогресираща;
- RMS (ремитентна множествена склероза).
"Betaferon" при пациенти с вторично прогресираща и рецидивираща множествена склероза намалява честотата (с 30%) и тежестта на клиничните екзацербации на патологията. Намалява броя на хоспитализациите и намалява нуждата от стероиди. Употребата на лекарството удължава ремисията.
При условие на лечение с Betaferon на пациенти, страдащи от вторично прогресираща множествена склероза, е възможно да се постигне успех в забавянето на по-нататъшното прогресиране на заболяването и появата на инвалидност.
Противопоказания
Свръхчувствителност към рекомбинантен или естествен бета-интерферон, както и човешки албумин.
Странични ефекти
- главоболие, гръдна болка, втрисане, коремна болка, некроза на мястото на инжектиране;
- миалгия, миастения гравис, крампи на краката;
- артериална хипертония;
- липса на координация, безсъние;
- задух, кожни лезии;
- наложително желание за уриниране, импотентност.
Лекарството не трябва да се приема по време на бременност или по време на кърмене.
специални инструкции
Лекарството съдържа човешки албумин, така че съществува риск от предаване на вирусни заболявания.
Преди започване и по време на лечението с Betaferon е необходимо да се направи подробен кръвен тест, включително брой на левкоцитите и тромбоцитите, и да се следи чернодробната функция. По време на лечението може да се наблюдава асимптоматично повишаване на нивото на чернодробните трансаминази, което е преходно.
Betaferon трябва да се предписва с повишено внимание на пациенти със сърдечна недостатъчност в стадий 3-4 (не са провеждани клинични проучвания). С развитието на фона на лечението на кардиомиопатия, лекарството се отменя.
На мястото на инжектиране понякога се появяват зони на некроза, които могат да се разпространят в дълбочина до мастната тъкан и мускулната фасция, което впоследствие води до развитие на белези. Понякога след това има нужда от отстраняване на участъци от некротична тъкан и присаждане на кожа. В случай на множествена некроза, лечението с Betaferon трябва да се преустанови.
Подробности за приложението са в инструкциите.
Сергей Михайленко 02.02.2016
Няколко пъти поръчах Betaferon в аптека Бурденко за майка ми. От няколко години тя страда от пристъпно-ремитентна множествена склероза. Всеки път бях доволен от обслужването. Доста бърза доставка, персоналът е спокоен и внимателен. Платих с куриер и в брой и MasterCard. Няма проблем. Доставката е безплатна, ако вземете лекарства на стойност 6000 рубли или повече.
Кира Фролова 05.03.2016гЗдравейте! В началото на април поръчах Betaferon в аптека Burdenko. Живеем в Ярославъл, но нашите аптеки нямат това лекарство. Трябваше да поръчам през интернет, малко се страхувах, че всичко ще бъде наред, иначе лекарството е скъпо. Рецептата трябваше да бъде сканирана и изпратена по имейл. Пратиха ми го по Unicom Cargo. Пратката пристигна за 2 дни. Плаща се наложен платеж.
Михаил Прокудин 14.04.2016 гКупих лекарството Betaferon в аптеката на Изследователския институт. Бурденко и получи 5% отстъпка. Дори не очаквах, че ако се регистрирате, можете да спестите. Лекарството ми беше доставено на адрес, платих с банкова карта. Рецептата беше помолена да бъде показана, въпреки факта, че я поръчах в интернет. В момента пия Betaferon. Ако поръчам отново, веднага ще се свържа тук.
Антивирусни - интерферони.
Състав Betaferon
Интерферон бета - 1b.
Производители
Boehringer Ingelheim Pharma KG, опаковано Schering AG (Германия)
фармакологичен ефект
Имуномодулиращи.
Интерферони, принадлежащи към семейството на цитокините, които са естествени протеини.
Интерферон бета-1b има антивирусно и имунорегулиращо действие.
Интерферон бета-1b намалява капацитета на свързване и експресията на рецепторите за гама-интерферон, засилва тяхното разпадане.
В допълнение, интерферон бета-1b повишава супресорната активност на мононуклеарните клетки на периферната кръв.
Странични ефекти на Betaferon
Депресивни състояния, тревожност, емоционална лабилност, деперсонализация, конвулсии, опити за самоубийство и объркване, има известни случаи на повишен мускулен тонус, възможна левкопения (лимфо-, неутропения), анемия, в редки случаи - тромбоцитопения, кардиомиопатия; в някои случаи - хипокалциемия, рядко - задух (след инжектиране), гадене, повръщане, когато се използва в препоръчваната доза - повишена активност на AST, ALT, гамаглутамил транспептидаза; описани са случаи на хепатит (предполага се лекарствена етиология), доста често при лечение в доза от 0,25 mg (8 000 000 IU), могат да се развият локални реакции - зачервяване, подуване, обезцветяване на кожата, възпаление, болка, свръхчувствителност, некроза, лимфаденопатия (с течение на времето при продължаване на лечението честотата на реакциите на мястото на инжектиране намалява).
В случай на нарушение на целостта на кожата, придружено от подуване или екстравазация на течност от мястото на инжектиране, пациентът трябва да се консултира с лекар.
В редки случаи се наблюдава алопеция, при жени, които не са достигнали менопауза, са възможни менструални нередности; в някои случаи - хиперурикемия, възможни са тежки реакции на свръхчувствителност (рядко - бронхоспазъм, анафилактичен шок, уртикария), сравнително често - грипоподобни симптоми (треска, втрисане, миалгия, неразположение или изпотяване), с течение на времето честотата на симптомите намалява; в редки случаи - дисфункция на щитовидната жлеза (хипер/хипотиреоидизъм).
Показания за употреба
Множествена склероза с рецидивиращ курс при наличие на поне две обостряния на заболяването през последните 2 години и последващо пълно или непълно възстановяване на неврологичните симптоми (за намаляване на честотата и тежестта на обострянията на заболяването при амбулаторни пациенти, които могат да се движат без помощ); вторично прогресиращ ход на множествена склероза (за намаляване на честотата и тежестта на екзацербациите, забавяне на прогресията на заболяването).
Противопоказания Betaferon
Анамнеза за свръхчувствителност към естествен или рекомбинантен интерферон бета или човешки албумин, анамнеза за тежка депресия и/или суицидни мисли, декомпенсирано чернодробно заболяване, епилепсия (неадекватно контролирана), бременност, кърмене.
Предозиране
При въвеждането на интерферон бета-1b в дози до 5,5 mg (176 милиона IU) интравенозно 3 пъти седмично при възрастни пациенти със злокачествени тумори не са наблюдавани сериозни животозастрашаващи нежелани реакции.
Взаимодействие
Може да се използва с кортикостероиди или аденокортикотропен хормон.
Интерфероните намаляват активността на чернодробните цитохром Р-450-зависими ензими.
Трябва да се внимава, когато се прилага в комбинация с лекарства, които имат тесен терапевтичен индекс, чийто клирънс до голяма степен зависи от чернодробната система на цитохром Р-450 (например антиепилептични лекарства).
Трябва да се внимава при едновременната употреба на всякакви лекарства, които засягат хемопоетичната система.
специални инструкции
Пациентите трябва да бъдат информирани за страничните ефекти на Betaferon.
Ако се появят депресия и мисли за самоубийство, терапията трябва да се спре незабавно.
Преди назначаването на Betaferon и по време на лечението трябва редовно да се извършва подробен кръвен тест, включително определяне на броя на левкоцитите, както и активността на ACT, ALT и гамаглутамил транспептидаза.
В случай на повишаване на активността на чернодробните трансаминази в кръвната плазма, трябва да се извърши внимателно наблюдение и изследване на пациента.
Лекарството трябва да се прекрати със значително повишаване на ензимната активност или появата на симптоми на хепатит.
За да намалите риска от развитие на некроза на мястото на инжектиране, трябва да спазвате правилата на асептиката при извършване на инжекции и постоянно да променяте местата на инжектиране.
За повече информация вижте инструкциите за медицинска употреба на лекарството.
Доза от
Лиофилизат за приготвяне на разтвор за подкожно приложение 0,3 mg (9,6 милиона IU) в комплект с разтворител
Състав
активно вещество - интерферон бета-1b - 0,3 mg (9,6 милиона IU)
с изчислено препълване от 20%,
помощни вещества: човешки албумин, манитол
Разтворител
1,2 ml от разтвора съдържат
активно вещество - натриев хлорид 6,48 mg,
помощни вещества - вода за инжекции.
Описание
Лиофилизат: лиофилизат с бял цвят
Разтворител: бистър разтвор, без частици.
Приготвен разтвор: леко опалесциращ до опалесциращ разтвор, безцветен до светложълт
Фармакотерапевтична група
Имуномодулатори. Имуностимуланти. Интерферони.
Интерферон бета-1b
ATX код L03AB08
Фармакологични свойства
Фармакокинетика
След подкожно приложение на Betaferon® в препоръчваната доза от 0,25 mg, серумните концентрации на интерферон бета-1b са ниски или изобщо не се откриват. В тази връзка няма информация за фармакокинетиката на лекарството при пациенти с множествена склероза, получаващи Betaferon® в препоръчваната доза.
След подкожно приложение на 0,5 mg Betaferon®, максималната плазмена концентрация се достига 1-8 часа след инжектирането и е около 40 IU / ml. Абсолютната бионаличност на Betaferon® при подкожно приложение е около 50%. При интравенозно приложение на интерферон бета-1b, клирънсът и полуживотът на лекарството от серума са средно 30 ml / min / kg и съответно 5 часа.
Въвеждането на Betaferon през ден не води до повишаване на нивото на лекарството в кръвната плазма и неговата фармакокинетика по време на лечението не се променя.
При подкожно приложение на Betaferon® в доза от 0,25 mg през ден, нивата на маркерите за биологичен отговор (неоптерин, бета2-микроглобулин и имуносупресивния цитокин IL-10) значително се повишават в сравнение с изходните стойности 6-12 часа след приложението. първа доза от лекарството. Те достигат пик на 40-124 часа и остават повишени за период от 7 дни (168 часа).
Фармакодинамика
Интерфероните се отнасят до цитокини, които са естествени протеини.
Интерферон бета-1b има антивирусно и имунорегулиращо действие. Механизмите на действие на интерферон бета-1b при множествена склероза не са напълно установени. Известно е обаче, че биологичният ефект на интерферон бета-1b се медиира от взаимодействието му със специфични рецептори, открити на повърхността на човешки клетки. Свързването на интерферон бета-1b с тези рецептори индуцира експресията на редица вещества, които се считат за медиатори на биологичните ефекти на интерферон бета-1b. Интерферон бета-1b намалява капацитета на свързване и експресията на рецепторите за гама-интерферон, засилва тяхното разпадане. В допълнение, интерферон бета-1b повишава супресорната активност на мононуклеарните клетки на периферната кръв.
Както при пристъпно-ремитентна, така и при вторично прогресираща множествена склероза, лечението с Betaferon® намалява честотата (с 30%) и тежестта на клиничните екзацербации на заболяването, броя на хоспитализациите и необходимостта от лечение със стероиди, а също така удължава продължителността на ремисията .
При пациенти с вторично прогресираща множествена склероза (МС), лечението с Betaferon® може да забави по-нататъшното прогресиране на заболяването и появата на увреждане, включително тежко увреждане (т.е. когато пациентите са принудени постоянно да използват инвалидна количка) до 12 месеца. Този ефект се наблюдава при пациенти с и без екзацербации на заболяването, както и с всеки индекс на увреждане (пациенти с резултат от 3,0 до 6,5 точки по разширената скала за увреждане EDSS).
Резултатите от ядрено-магнитен резонанс на мозъка на пациенти с рецидивираща и вторично прогресираща множествена склероза по време на лечение с Betaferon® потвърждават значителния положителен ефект на лекарството върху тежестта на патологичния процес, както и значително намаляване на образуването на нови активни огнища.
Лечението с Betaferon® при пациенти след първите клинични прояви на множествена склероза (клинично изолиран синдром) може да намали риска от развитие на значителна множествена склероза с 50% и да увеличи периода до развитие на значима множествена склероза средно с 363 дни.
Показания за употреба
Пациенти с първи прояви на демиелинизация, с активен възпалителен процес, достатъчно тежък, за да оправдае терапия с интравенозни кортикостероиди, при условие че се изключат алтернативни диагнози и се установи висок риск от развитие на сигурна множествена склероза (вижте раздел Фармакодинамични свойства)
Пациенти с пристъпно-ремитентна множествена склероза (RRMS) с най-малко 2 екзацербации през последните 2 години
Пациенти с вторично прогресираща множествена склероза, с активен ход на заболяването, характеризиращ се с екзацербации.
Дозировка и приложение
Лечението с Betaferon® трябва да се провежда под наблюдението на лекар с опит в лечението на множествена склероза.
Въвеждането на лекарството
Начин на приложение: за подкожни инжекции
Приготвяне на инжекционен разтвор
За разтваряне на лиофилизата използвайте предоставената готова спринцовка с разтворител и адаптер за флакон с игла. 1,2 ml разтворител (0,54% разтвор на натриев хлорид) се инжектира в бутилка с Betaferon®. Лиофилизатът трябва да се разтвори напълно, без да се разклаща.
След разтваряне изтеглете 1 ml от разтвора от флакона в спринцовката, за да инжектирате 0,25 mg Betaferon®.
Разкачете спринцовката от флакона и адаптера преди инжектиране. Betaferon® може да се прилага с помощта на подходящ автоинжектор.
Не използвайте повредени флакони.
Преди употреба проверете готовия разтвор. При наличие на частици или промяна в цвета на разтвора, той не трябва да се използва и трябва да се унищожи.
Лекарството трябва да се прилага подкожно веднага след приготвяне на разтвора. Ако инжекцията се забави, разтворът трябва да се съхранява в хладилник и да се използва в рамките на 3 часа.Разтворът не трябва да се замразява.
Пациентите трябва да започнат с начална доза от 62,5 микрограма (0,25 ml) подкожно през ден и бавно да увеличат дозата до 250 микрограма (1,0 ml) през ден (подробности за употребата на опаковката за титриране са в приложението).
Продължителността на времето за титруване се определя индивидуално в зависимост от поносимостта.
Схема за титриране на дозата*
*Схемата на титриране може да се коригира, ако възникнат значителни нежелани реакции
Оптималната доза на лекарството не е напълно определена.
Понастоящем въпросът за продължителността на лечението с Betaferon® остава нерешен.
При контролирани условия, при пациенти с пристъпно-ремитентна множествена склероза, курсът на лечение с Betaferon® е до 5 години, а при пациенти с вторично прогресираща множествена склероза курсът е до 3 години.
При пациенти с пристъпно-ремитентна множествена склероза е доказана ефикасност през първите 2 години от лечението с лекарството. Наличните данни за следващите 3 години лечение съответстват на данните за ефективността на лечението с Betaferon® за целия период на дългосрочно лечение.
При пациенти с първи клинични прояви със съмнение за множествена склероза, развитието на значима множествена склероза значително се забави по време на 5-годишно лечение с Betaferon®.
Лечението с Betaferon® не се препоръчва при пациенти с пристъпно-ремитентна множествена склероза, които имат анамнеза за по-малко от 2 екзацербации през последните 2 години или при пациенти с вторично прогресираща множествена склероза, които не са имали екзацербация на заболяването през последните 2 години. години.
Лечението с Betaferon трябва да се преустанови, ако пациентът не реагира на лечението, например ако има стабилна прогресия на симптомите по скалата EDSS в продължение на 6 месеца или в случаите, когато са проведени най-малко 3 курса на лечение с адренокортикотропен хормон (ACTH) или кортикостероиди бяха необходими в рамките на една година.
Странични ефекти
В началото на лечението нежеланите реакции са чести, но по правило честотата им намалява с времето по време на лечението. Най-често наблюдаваните нежелани реакции са комплекс от грипоподобни симптоми (треска, втрисане, артралгия, неразположение, изпотяване, главоболие и миалгия), които се дължат главно на фармакологичните ефекти на лекарството, както и реакции при инжектиране. сайт. Реакциите на мястото на инжектиране се появяват често след приложение на Betaferon®. Зачервяване, локален оток, обезцветяване на кожата, възпаление, болка, свръхчувствителност, некроза и неспецифични реакции са до голяма степен свързани с лечението с Betaferon® 250 mcg (8 милиона IU). За да се подобри поносимостта на Betaferon®, обикновено се препоръчва титриране на дозата в началото на лечението. Появата на грипоподобни симптоми може да бъде намалена и чрез прилагане на нестероидни противовъзпалителни средства. Използването на автоинжектор намалява честотата на реакциите на мястото на инжектиране.
Нежеланите реакции, изброени по-долу, се основават на данни от клинични проучвания и постмаркетингови наблюдения. Честотата на нежеланите реакции, наблюдавани по време на употребата на Betaferon®, е дадена по-долу в съответствие със следната градация: много чести (³1/10) и чести (³1/100 до<1/10), нечастые (³1/1000 до <1/100, редкие (³1/10000 до <1/1000) и очень редкие (1/10000).
Най-подходящият термин на MedDRA се използва за описание на определени реакции и техните синоними и свързани състояния.
С неизвестна честота:
Индуциран от лекарства лупус-подобен синдром (еритематоза)
Известие за подозирана нежелана реакция
Много е важно да докладвате подозирана нежелана реакция след пускането на лекарството на пазара. Това позволява дългосрочно проследяване на съотношението полза/риск на лекарствения продукт. Здравните специалисти трябва да бъдат уведомени за всяка подозирана нежелана реакция.
Противопоказания
Започване на лечение по време на бременност
Реакции на свръхчувствителност към естествени или рекомбинантни
интерферон-бета или други помощни вещества на лекарството в
история
Наличие на настояща тежка депресия и/или суицидни мисли
Чернодробни заболявания в стадия на декомпенсация
Лекарствени взаимодействия
Не са провеждани специални проучвания за взаимодействието на Betaferon® с други лекарства.
Ефектът на Betaferon® при 250 mcg (8 милиона единици) през ден върху метаболизма на други лекарства при пациенти с множествена склероза не е известен.
На фона на употребата на Betaferon®, кортикостероидите и ACTH, предписани до 28 дни при лечение на екзацербации, се понасят добре.
Поради недостатъчен клиничен опит при пациенти с множествена склероза, не се препоръчва употребата на Betaferon® едновременно с други имуномодулатори, в допълнение към кортикостероидите или ACTH.
Интерфероните намаляват активността на чернодробните цитохром Р450-зависими ензими при хора и животни. Ето защо трябва да се внимава, когато се предписва Betaferon® в комбинация с лекарства, които имат тесен терапевтичен индекс, чийто клирънс до голяма степен зависи от чернодробната система на цитохром Р450 (например антиепилептични лекарства). Също така трябва да се внимава при едновременната употреба на всякакви лекарства, които засягат хемопоетичната система.
Не са провеждани специални проучвания за взаимодействие с антиепилептични лекарства.
специални инструкции
Имунни нарушения
Употребата на цитокини при пациенти с моноклонална гамапатия (рядко заболяване на имунната система, характеризиращо се с появата на абнормни протеини в кръвта) понякога е придружено от системно повишаване на пропускливостта на капилярите със симптоми, подобни на шок, и смърт.
· Стомашно-чревни нарушения
По време на употребата на Betaferon® в редки случаи са наблюдавани случаи на панкреатит, често придружен от хипертриглицеридемия.
Нарушения на нервната система
Betaferon® трябва да се прилага с повишено внимание при пациенти с анамнеза за депресивни разстройства или налични, по-специално суицидни мисли. Както е известно, депресията и суицидните мисли са по-чести в популацията на пациенти с множествена склероза, включително по време на лечение с интерферони. Пациентите, които са показани за лечение с Betaferon®, трябва да бъдат информирани, че по време на лечението с лекарството могат да се появят депресивни разстройства и суицидни мисли, които трябва незабавно да бъдат докладвани на лекуващия лекар. В редки случаи тези симптоми могат да доведат до опити за самоубийство. Пациентите с прояви на депресия и мисли за самоубийство трябва да бъдат под строго медицинско наблюдение. Ако е необходимо, трябва да се обмисли прекратяване на лечението при такива пациенти.
Betaferon трябва да се използва с повишено внимание при пациенти с анамнеза за гърчове и при пациенти, получаващи антиепилептично лечение, особено когато епилептичните гърчове не се контролират адекватно от антиепилептични лекарства.
Препаратът съдържа човешки албумин и поради тази причина съществува потенциален риск от предаване на вирусни заболявания. Рискът от предаване на болестта на Кройцфелд-Якоб не може да бъде изключен.
Промени в лабораторните показатели
Пациентите с дисфункция на щитовидната жлеза се съветват да проверяват функцията на щитовидната жлеза редовно и в противен случай според клиничните показания.
В допълнение към стандартните лабораторни изследвания, предписани при лечението на пациенти с множествена склероза, преди започване на лечението и редовно по време на лечението с Betaferon®, а след това периодично при липса на клинични симптоми, се препоръчва извършването на подробен кръвен тест, включително определяне на броя на левкоцитите, броя на тромбоцитите и химията на кръвта, както и проверка на чернодробната функция (напр. активност на аспартат аминотрансфераза (AST), аланин аминотрансфераза (ALT) и гамаглутамилтрансфераза (GT).
При лечение на пациенти с анемия, тромбоцитопения, левкопения (единична или комбинирана) може да се наложи по-внимателно проследяване на пълна кръвна картина, включително диференциален анализ и брой на тромбоцитите.
Нарушения на черния дроб и жлъчните пътища
По време на лечението с Betaferon® може да настъпи асимптоматично повишаване на серумните трансаминази, в повечето случаи леко и преходно.
Както при другите бета-интерферони, тежко чернодробно увреждане (включително чернодробна недостатъчност) е рядко при Betaferon. Най-тежкото чернодробно увреждане възниква по-често при пациенти, приемащи лекарства или вещества, свързани с хепатотоксичност, или при наличие на съпътстващи заболявания (напр. метастатично злокачествено заболяване, тежки инфекции и сепсис, злоупотреба с алкохол).
При наблюдение на пациенти трябва да се обърне внимание на признаци, показващи нарушена чернодробна функция. При повишена активност на серумните трансаминази се препоръчва наблюдение и изследване на пациента. При значително повишаване на активността на чернодробните ензими или когато това увеличение е съчетано с клинични симптоми, като жълтеница, трябва да се обмисли необходимостта от прекратяване на лечението с Betaferon®. С изчезването на клиничните признаци на нарушена чернодробна функция и след нормализиране на нивото на чернодробните ензими трябва да се обмисли възможността за възобновяване на терапията с подходящо проследяване на чернодробната функция.
・Нарушения на бъбреците и пикочните пътища
Трябва да се внимава и е необходимо внимателно наблюдение, когато се предписва лекарството при пациенти с тежка бъбречна недостатъчност.
нефротичен синдром
По време на лечение с бета-интерферон са докладвани случаи на нефротичен синдром под формата на големи нефропатии, включително фокална сегментна гломерулосклероза, липоидна нефроза, мембранопролиферативен гломерулонефрит и мембранозна гломерулопатия.Тези заболявания са наблюдавани по различно време по време на лечението и могат да се появят след няколко години използване на бета-интерферон.
Препоръчва се редовно проследяване за ранни признаци или симптоми като оток, протеинурия или нарушена бъбречна функция, особено при пациенти с висок риск от бъбречно заболяване. Нефротичният синдром трябва да се лекува незабавно и трябва да се обмисли прекратяване на лечението с Betaferon®
Заболявания на сърдечно-съдовата система
Betaferon® трябва да се прилага с повишено внимание при пациенти със сериозно сърдечно заболяване като застойна сърдечна недостатъчност, коронарна артериална болест или аритмии. Въпреки че няма данни за директен кардиотоксичен ефект на Betaferon®, тези пациенти трябва да бъдат наблюдавани за влошаване на сърдечните състояния. Betaferon® няма известен директен кардиотоксичен ефект, но грипоподобните симптоми, обикновено свързани с употребата на бета-интерферони, причиняват стрес върху сърцето поради висока температура, втрисане, тахикардия. Това може да влоши симптомите при пациенти със сериозно сърдечно заболяване. Според постмаркетинговия опит при пациенти със сериозно сърдечно заболяване, в редки случаи се съобщава за влошаване на сърдечната функция във времева връзка с началото на лечението с Betaferon®.
В редки случаи се съобщава за развитие на кардиомиопатия. С развитието на кардиомиопатия и възможната му връзка с употребата на Betaferon®, лечението с лекарството трябва да се преустанови.
Тромботична микроангиопатия (ТМА)
По време на лечение с препарати с интерферон бета са докладвани случаи на тромботична микроангиопатия, проявяваща се като тромботична тромбоцитопенична пурпура или хемолитичен уремичен синдром, включително фатални случаи.
Тези усложнения се появяват по различно време по време на лечението и могат да се появят седмици до години след започване на лечението с интерферон-бета.
Ранните клинични симптоми на заболяването включват тромбоцитопения, внезапна поява на хипертония, треска, признаци на нарушения на централната нервна система (напр. объркване, пареза) и нарушена бъбречна функция.
Резултатите от лабораторните тестове, предполагащи възможността за TMA, включват намаляване на броя на тромбоцитите, повишаване на серумната лактат дехидрогеназа (LDH) поради хемолиза и шистоцити (фрагменти от червени кръвни клетки) в кръвна натривка.
Съответно, при откриване на клинични симптоми на ТМА се препоръчва да се проведе изследване на нивото на тромбоцитите и LDH в серума, кръвна намазка и показатели за бъбречна функция. Ако се потвърди TMA, трябва да се проведе незабавно лечение (включително плазмафереза) и трябва да се обмисли възможността за незабавно спиране на лечението с Betaferon®.
Общи нарушения и състояние на мястото на инжектиране
Могат да възникнат тежки реакции на свръхчувствителност (тежки остри реакции като бронхоспазъм, анафилаксия и уртикария).
При пациенти, лекувани с Betaferon®, има случаи на некроза на мястото на инжектиране. Некрозата може да бъде обширна и да обхване мускулната фасция, както и мастния слой и в резултат на това да доведе до образуване на белези. В някои случаи е необходимо отстраняване на мъртва кожа или, по-рядко, присаждане на кожа. Лечебният процес може да отнеме до 6 месеца.
Ако пациентът има увреждане на целостта на кожата, което може да бъде свързано с подуване или изтичане на течност от мястото на инжектиране, е необходимо да се свържете с лекуващия лекар, преди да продължите с инжекциите Betaferon®.
Когато се появят множество огнища на некроза, лечението с Betaferon® трябва да се преустанови до пълното заздравяване на увредените участъци. При наличие на един фокус, ако некрозата не е твърде обширна, употребата на Betaferon® може да продължи, тъй като при някои пациенти заздравяването на мъртвата зона на мястото на инжектиране е настъпило по време на употребата на Betaferon®.
За да се намали рискът от развитие на реакция и некроза на мястото на инжектиране, пациентите трябва да бъдат посъветвани да:
Извършвайте инжекции при стерилни условия;
Сменяйте мястото на инжектиране всеки път;
Инжектирайте лекарството строго подкожно.
Периодично трябва да се следи правилността на извършването на независими инжекции, особено ако възникнат реакции на мястото на инжектиране.
Честотата на реакциите на мястото на инжектиране (например зачервяване, локален оток, обезцветяване на кожата, възпаление, болка, свръхчувствителност, некроза и неспецифични реакции) обикновено намалява с времето при продължаване на лечението. Използването на автоинжектор намалява честотата на реакциите на мястото на инжектиране.
Имуногенност/неутрализиращи антитела
Както при други лекарства с протеинова природа, има възможност за развитие на имуногенност. При контролирани клинични проучвания на всеки 3 месеца са вземани серумни проби, за да се наблюдава развитието на антитела срещу Betaferon®.
В различни контролирани клинични изпитвания при пристъпно-ремитентна множествена склероза и вторично прогресираща множествена склероза, 23-41% от пациентите развиват неутрализираща активност към интерферон бета-1b, което се потвърждава от поне два последователни положителни титъра.
Между 43% и 55% от тези пациенти са прогресирали до стабилен отрицателен статус (въз основа на два последователни отрицателни титъра) по време на периода на проследяване на съответното проучване.
Развитието на неутрализираща активност в тези проучвания е свързано с намаляване на клиничната ефикасност само във връзка с екзацербациите.
Смята се, че този ефект може да бъде по-изразен при пациенти с по-високи титри на неутрализираща активност.
В проучване на пациенти с първи симптоми със съмнение за множествена склероза, неутрализиращата активност, измервана на всеки 6 месеца, е наблюдавана при най-малко 32% (89) от пациентите, първоначално лекувани с Betaferon®. От тях 60% (53) са имали връщане към отрицателен статус при последната оценка за период от 5 години. В рамките на този период развитието на неутрализираща активност е свързано със значително увеличаване на новите активни лезии и обема на Т2 лезиите по време на магнитно резонансно изображение. Това обаче не е свързано с намаляване на клиничната ефикасност (по отношение на времето до определена МС), времето до потвърдена прогресия на EDSS симптома и честотата на рецидивите).
Няма нежелани реакции, свързани с развитието на неутрализираща активност.
Проучвания in vitro показват, че Betaferon® реагира кръстосано с интерферон-бета от естествен произход. Тъй като не са провеждани in vivo проучвания, клиничното му значение не е ясно.
Има редки и неубедителни данни при пациенти, които са развили неутрализираща активност и са завършили лечението с Betaferon®.
Решението за продължаване на лечението с Betaferon® се основава на всички аспекти на болестния статус на пациента, а не на състоянието на неутрализираща активност поотделно.
Приложение в педиатрията
Не са провеждани официални клинични изпитвания или фармакокинетични проучвания при деца и юноши. Ограничените публикувани данни обаче предполагат, че профилът на безопасност при юноши на възраст от 12 до 16 години при използване на Betaferon® 8,0 милиона IU подкожно през ден е подобен на профила на безопасност при възрастни. Няма информация за употребата на Betaferon при деца под 12-годишна възраст. Betaferon не трябва да се използва в тази възрастова група.
Бременност и кърмене
Данните за употребата на Betaferon® по време на бременност са ограничени. Има съобщения за спонтанни аборти при жени с множествена склероза. Започването на терапия по време на бременност е противопоказано (вижте точка "Противопоказания")
Жените в репродуктивна възраст трябва да използват надеждни методи за контрацепция по време на лечението с лекарството. В случай на бременност по време на лечение с Betaferon® или планирана бременност, жената трябва да бъде информирана за потенциалния риск и се препоръчва да се преустанови употребата на лекарството. При пациенти с висока честота на екзацербации преди лечението, рискът от тежко обостряне след преустановяване на лечението с Betaferon® в началото на бременността трябва да се прецени спрямо възможния повишен риск от спонтанен аборт.
Не е известно дали интерферон бета-1b се екскретира в кърмата.
Като се има предвид теоретичната възможност за развитие на нежелани реакции към Betaferon® при кърмачета, е необходимо да се спре кърменето или да се спре лекарството.
Характеристики на ефекта на лекарството върху способността за шофиране на превозни средства и потенциално опасни механизми
Не са провеждани специални проучвания за ефекта на лекарството върху способността за шофиране и работа с механизми. Развитието на нежелани реакции от нервната система на фона на употребата на Betaferon® може да повлияе на способността за шофиране и работа с механизми при чувствителни пациенти.
Предозиране
Не е идентифициран. Интерферон бета-1b е прилаган на възрастни пациенти с рак във високи дози от порядъка на 5500 mcg (176 милиона IU) интравенозно три пъти седмично без развитие на сериозни странични ефекти, засягащи жизнените функции.
Да се пази извън обсега на деца!
Срок на годност
Лиофилизат - 2 години
Разтворител - 3 години
Да не се използва след изтичане срока на годност на лекарството.
Условия за отпускане от аптеките
По лекарско предписание
производител
Boehringer Ingelheim Pharma GmbH & Co. KG, Германия
88397 Биберах ан дер Рис, Германия
Catad_pgroup Лекарства за множествена склероза
Betaferon - инструкции за употреба
РЕГИСТРАЦИОНЕН НОМЕР:
ТЪРГОВСКО НАИМЕНОВАНИЕ НА ЛЕКАРСТВОТО:
Бетаферон
МЕЖДУНАРОДНО НЕПАТЕНТНО ИМЕ:
Интерферон бета-1b
ЛЕКАРСТВЕНА ФОРМА:
Лиофилизат за приготвяне на разтвор за подкожно приложение
СЪСТАВ
Всеки флакон с активното вещество съдържа: Интерферон бета-1b (IFN-beta-1b) - 0,30 mg (съответства на 9,6 милиона IU), човешки албумин - 15,00 mg, манитол - 15,00 mg.
1 ml от приготвения разтвор съдържа 0,25 mg (8,0 милиона IU) рекомбинантен интерферон бета-1b.
1 ml воден разтворител за инжекционен разтвор съдържа 5,4 mg натриев хлорид.
ОПИСАНИЕ
Лиофилизат: Лиофилизирана маса с бял цвят.
Разтворител: Бистър, почти безцветен разтвор.
Приготвен разтвор: Леко опалесциращ до опалесциращ разтвор, безцветен или светложълт.
ФАРМАКОТЕРАПЕВТИЧНА ГРУПА
цитокин. Средства за лечение на множествена склероза.
ATH КОД: L03AB08
ФАРМАКОЛОГИЧНИ СВОЙСТВА
Фармакодинамика
Интерфероните са протеини, принадлежащи към семейството на цитокините и имащи молекулно тегло от 15 000 до 21 000 далтона. Има три класа интерферони: интерферон алфа, интерферон бета и интерферон гама, които имат различни, но припокриващи се биологични активности. Активността на интерферон бета-1b е видоспецифична, така че най-подходящата фармакологична информация за интерферон бета-1b може да бъде получена от проучвания с култивирани човешки клетки или in vivo изследвания при хора.
Активното вещество на лекарството Betaferon (интерферон бета-1b) има антивирусно и имуномодулиращо действие. Механизмите на действие на интерферон бета-1b при множествена склероза (МС) не са напълно установени. Известно е обаче, че биологичният ефект на интерферон бета-1b се медиира от взаимодействието му със специфични рецептори, открити на повърхността на човешки клетки. Свързването на интерферон бета-1b с тези рецептори индуцира експресията на редица вещества, които се считат за медиатори на биологичните ефекти на интерферон бета-1b. Съдържанието на някои от тези вещества е определено в серума и фракциите на кръвните клетки на пациенти, лекувани с интерферон бета-1b. Интерферон бета-1b намалява капацитета на свързване и също така подобрява интернализацията и разграждането на рецепторите за гама-интерферон. В допълнение, интерферон бета-1b повишава супресорната активност на мононуклеарните клетки на периферната кръв. Не са провеждани отделни проучвания за ефекта на Betaferon върху сърдечно-съдовата, дихателната и ендокринната система.
Клинични изследвания:
Пристъпно-ремитентна множествена склероза
В клинично проучване, проведено при пациенти с пристъпно-ремитентна множествена склероза и способни да се движат без чужда помощ (изходна EDSS стойност от 0 до 5,5), е показано, че лечението с Betaferon намалява честотата (с 30%) и тежестта на клиничните екзацербации на заболяване, броя на хоспитализациите поради заболяването, а също така удължава продължителността на ремисията. Няма информация за ефекта на терапията с Betaferon върху продължителността на рецидива или появата на симптомите между екзацербациите, както и върху прогресията на заболяването при пристъпно-ремитентна множествена склероза.
Вторично прогресираща множествена склероза:
Проведени са две контролирани клинични изпитвания при 1657 пациенти с вторично прогресираща МС (изходен EDSS 3 до 6,5, т.е. пациенти, способни да ходят). Пациенти с леко заболяване, както и пациенти с неподвижност, не са включени в проучванията. Резултатите от двете проучвания показват противоречиви резултати за първичната крайна точка, времето до потвърдена прогресия на заболяването, за забавяне на прогресията на увреждането.
В едно от двете проучвания, по време на лечение с Betaferon, е доказано статистически значимо забавяне на прогресията на увреждането (коефициент на риск = 0,69, 95% доверителен интервал (0,55; 0,86), p = 0,0010 съответства на намаление на риска от 31% в резултат на терапия с Betaferon) и тежко увреждане (т.е. когато пациентите са принудени постоянно да използват инвалидна количка) (коефициент на риск = 0,61, 95% доверителен интервал (0,44; 0,85), p = 0,0036 съответства на намаляване на риска с 39%, тъй като резултат от терапия с Betaferon). Този ефект се наблюдава в продължение на 33 месеца при пациенти с какъвто и да е индекс на увреждане, независимо от честотата на рецидивите. Във второ проучване, включващо пациенти с вторично прогресираща МС, не е имало забавяне на настъпването на увреждане в резултат на лечение с Betaferon. Има доказателства, че пациентите, включени в това проучване, са били в по-малко активен стадий на заболяването в сравнение с пациентите, участвали в първото проучване.
Данните от ретроспективен мета-анализ на двете проучвания показват общ статистически значим ефект от терапията (p = 0,0076; 8 милиона IU Betaferon в сравнение с пациенти, получаващи плацебо).
Ретроспективен анализ на подгрупи показа, че лечението с Betaferon има по-голяма вероятност да окаже влияние върху времето до настъпване на увреждане при пациенти с активно заболяване преди терапията (коефициент на риск 0,72, 95% доверителен интервал (0,59; 0,88), p= 0,0011 съответстват на 28% намаление на риска в резултат на терапия с Betaferon при пациенти с рецидиви или тежка прогресия на EDSS, 8 милиона IU Betaferon в сравнение с пациенти, лекувани с плацебо). Ретроспективни данни предполагат, че рецидивите, както и подчертаната прогресия на EDSS (EDSS >1 или EDSS >0,5 за EDSS >6 през предходните две години) могат да помогнат за идентифициране на пациенти с активно заболяване.
И в двете проучвания при пациенти с вторично прогресираща множествена склероза лечението с Betaferon намалява честотата на клиничните екзацербации с 30%. Няма данни за ефекта на терапията върху продължителността на рецидивите.
Клинично изолиран синдром, предполагащ множествена склероза
Едно контролирано клинично проучване е проведено при пациенти с клинично изолиран синдром и находки от мозъчен магнитен резонанс (MRI), предполагащи множествена склероза (най-малко две лезии, които не са клинично видими на T2-претеглени MRI изображения). Проучването включва пациенти с монофокално или мултифокално начало на заболяването (т.е. пациенти с клинични прояви на една или поне две лезии на централната нервна система). Пациенти със симптоми на някакво заболяване, подобни на тези на множествена склероза, бяха изключени от проучването.
Това проучване включва 2 фази: плацебо-контролирана фаза (плацебо срещу Betaferon), последвана от предварително планирана фаза на проследяване. Плацебо-контролираната фаза е продължила 2 години или до развитието на клинично значима множествена склероза (MSMS), което от двете настъпи първо. След завършване на плацебо-контролираната фаза на проучването, пациентите влизат в предварително планирана фаза на проследяване, за да сравнят ефектите от ранното спрямо късното започване на терапия с Betaferon. Направени са сравнения между пациенти, първоначално рандомизирани на Betaferon (група за ранно започване на бетаферон) и плацебо (група за късно започване).
Маса 1.
РПървични резултати за ефикасност, базирани на данни от проучването ПОЛЗА и резултатите от проследяването според проучванетоПОЛЗА последвам- нагоре.

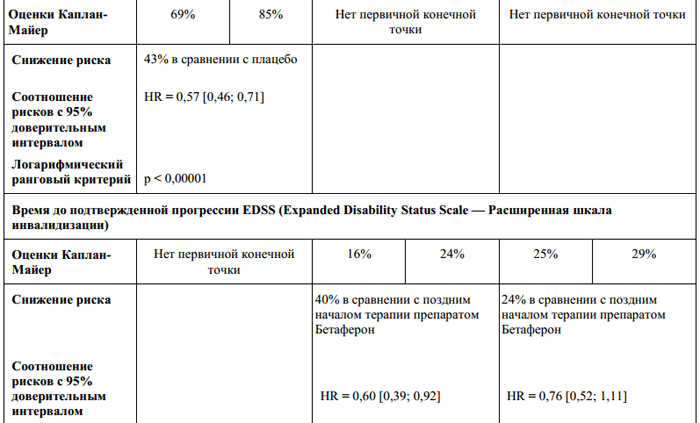
В плацебо-контролираната фаза на проучването Betaferon забавя прогресията на заболяването от първата клинична изява до клинично значима множествена склероза. Терапията с Betaferon причинява стабилно забавяне на прогресията на множествената склероза според критериите на McDonald (Таблица 1).
Лечението с Betaferon има ефект върху прогресията на заболяването до CRMS във всички анализирани подгрупи. Пациенти с монолезионна форма и най-малко девет лезии на Т2-претеглени изображения или Gd-усилване на изходно ниво на MRI на мозъка са имали повишен риск от прогресия на заболяването до CRMS в рамките на 2 години. При пациенти с мултифокална форма, времето на развитие на заболяването преди CRMS не зависи от първоначалните параметри на ЯМР, което се основава на
клиничните наблюдения показват висок риск от CRMS порадипрогресия на заболяването. В момента няма ясна дефиниция
дефиниране на понятието "висок риск". По-консервативен подход би бил да се идентифицират най-малко девет хиперинтензивни лезии на Т2-претеглени изображения при първоначалното сканиране и поне една нова лезия на Т2-претеглени изображения или една нова Gd-усилена лезия поне един месец след първоначалното сканиране. . Във всеки случай лечението трябва да се прилага само при пациенти с висок риск.
Високият процент пациенти, завършили проучването (93% от групата на Betaferon), показва, че лечението с Betaferon се понася добре. За да се увеличи поносимостта на лекарството в началото на терапията, се извършва титриране на дозата и въвеждане на нестероидни противовъзпалителни средства. Освен това, по време на цялото проучване, по-голямата част от пациентите са приемали лекарството с помощта на автоинжектор.
В последващата фаза на открито наблюдение ефектът от терапията след 3 и 5 години лечение е очевиден (Таблица 1), дори ако повечето пациенти в групата на плацебо са получавали лечение с Betaferon поне от втората година на заболяването. В групата с ранно лечение с Betaferon (Таблица 1, изразен ефект след 3 години, без значим ефект след 5 години), прогресията на заболяването по скалата EDSS (потвърдено увеличение на EDSS с поне една точка в сравнение с изходното ниво) е по-ниска. По-голямата част от пациентите и в двете групи не са имали прогресия на увреждането в рамките на 5 години. За "ранно започване на терапия" не е демонстриран устойчив ефект върху тази изходна линия. Не са открити ползи по отношение на качеството на живот, както е определено в съответствие с FAMS (Функционална оценка на МС - функционална оценка на множествена склероза: индекс на лечение, резултат), поради ранното започване на терапия с Betaferon.
Пристъпно-ремитентна множествена склероза, вторично прогресираща множествена склероза и клинично изолиран синдром, предполагащ множествена склероза.
Резултатите от MRI при пациенти с множествена склероза показват ефективността на лекарството Betaferon и забавяне на хода на заболяването във всички проучвания. Според резултатите от оценката на ЯМР връзката между хода на множествената склероза и клиничния резултат все още не е изяснена.
Токсикологична характеристика
Не са провеждани проучвания за остра токсичност. Тъй като гризачите са нечувствителни към ефектите на човешкия интерферон бета, оценката на риска се основава на проучвания за токсичност при многократни дози при маймуни резус. Наблюдава се преходна хипертермия, заедно с изразено преходно повишаване на концентрацията на лимфоцити и преходно намаляване на тромбоцитите и сегментираните неутрофили.
Не са провеждани дългосрочни проучвания за токсичност. Проучванията за репродуктивна токсичност при маймуни резус показват токсичност за майката и увеличаване на честотата на спонтанните аборти. Не са наблюдавани малформации в живо потомство. Не са провеждани проучвания за ефекта върху фертилитета. Не е наблюдаван ефект върху естралния цикъл на маймуните.
В едно отделно проучване за генотоксичност (тест на Ames) не са наблюдавани мутагенни ефекти. Не са провеждани проучвания за канцерогенност. In vitro тест за клетъчна трансформация не разкрива никакъв канцерогенен потенциал.
Фармакокинетика
Плазмената концентрация на интерферон бета-1b при пациенти и доброволци се определя с помощта на специфичен биологичен анализ.
След подкожно инжектиране на 0,5 mg (16,0 милиона IU) интерферон бета-1b, максималната плазмена концентрация се достига 1-8 часа след инжектирането и е около 40 IU / ml. Според различни проучвания, при интравенозно приложение на интерферон бета-1b, клирънсът и неговият полуживот от плазмата са средно 30 ml / min / kg и съответно 5 часа.
Въвеждането на лекарството Betaferon през ден не води до повишаване на концентрацията на интерферон бета-1b в кръвната плазма и неговата фармакокинетика по време на лечението не се променя.
При подкожно приложение на интерферон бета-1b абсолютната бионаличност е приблизително 50%.
ПОКАЗАНИЯ ЗА УПОТРЕБА
Клинично изолиран синдром (CIS) (единственият клиничен епизод на демиелинизация, предполагащ множествена склероза, при изключване на алтернативни диагнози) с достатъчна тежест на възпалителния процес за предписване на интравенозни кортикостероиди - за
забавяне на прехода към клинично значима множествена склероза (CRMS) при пациенти с висок риск от развитие на CRMS.
Няма общоприето определение за висок риск. Според проучването, пациентите с монофокална CIS (клинични прояви на 1 лезия в ЦНС) и ≥ 9 фокуса на Т2-претеглени изображения на ЯМР и/или фокуси, натрупващи контрастен агент, са изложени на висок риск от развитие на CRMS. Пациентите с мултифокална CIS (клинични прояви на >1 лезия в ЦНС) са изложени на висок риск от развитие на CRMS, независимо от броя на огнищата при MRI.
Пристъпно-ремитентна множествена склероза (RRMS) - за намаляване на честотата и тежестта на екзацербациите при амбулаторни пациенти (т.е. пациенти, способни да ходят без помощ) с анамнеза за най-малко 2 екзацербации през последните две години, последвани от пълно или непълно възстановяване на неврологичен дефицит.
Вторично прогресираща множествена склероза с активен ход на заболяването, характеризиращ се с екзацербации или изразено влошаване на неврологичните функции през последните две години - за намаляване на честотата и тежестта на клиничните екзацербации на заболяването, както и за забавяне на скоростта на прогресия на болестта.
ПРОТИВОПОКАЗАНИЯ
- Бременност
- Кърмене.
- Реакции на свръхчувствителност към естествен или рекомбинантен интерферон бета в историята и компонентите, които съставляват лекарството.
- Тежка депресия и/или суицидни мисли.
- Чернодробни заболявания в стадия на декомпенсация.
- Деца под 18-годишна възраст (информацията за ефикасността и безопасността на употребата на интерферон бета-1b при деца е ограничена).
ВНИМАТЕЛНО
Betaferon трябва да се използва с повишено внимание при пациенти със следните състояния:
- сърдечни заболявания, по-специално сърдечна недостатъчност III-IV функционален клас според класификацията на New York Heart Association (NYHA), кардиомиопатия;
- анамнеза за епилептични припадъци;
- моноклонална гамапатия;
- анемия, тромбоцитопения, левкопения;
- тежка бъбречна недостатъчност.
УПОТРЕБА ПРИ БРЕМЕННОСТ И ПО ВРЕМЕ НА КЪРМЕНЕ
Бременност
Има ограничена информация за потенциала на Betaferon да причини увреждане на плода при лечение на бременни жени или да повлияе на човешката репродуктивна функция. При контролирани клинични проучвания при пациенти с множествена склероза има случаи на спонтанен аборт. Употребата на Betaferon по време на бременност е противопоказана.
Жените в репродуктивна възраст по време на лечението с Betaferon трябва да използват надеждни методи за контрацепция. В случай на бременност по време на лечението или при планиране на бременност пациентката трябва да бъде информирана за потенциалния риск за плода. В този случай се препоръчва да се отмени употребата на Betaferon.
При пациенти с висок процент на рецидиви в историята, преди започване на терапията, е необходимо да се оцени рискът от развитие на сериозен рецидив след спиране на лечението с лекарството по време на бременност спрямо възможния риск от спонтанен аборт.
период на кърмене
Не е известно дали интерферон бета-1b се екскретира в кърмата. Като се има предвид теоретичната възможност за развитие на нежелани реакции към лекарството Betaferon при кърмачета, които са кърмени, е необходимо да се спре кърменето или да се преустанови лекарството.
НАЧИН НА ПРИЛОЖЕНИЕ И ДОЗИ
Терапията с Betaferon трябва да започне под наблюдението на лекар с опит в лечението на множествена склероза.
В началото на лечението обикновено се препоръчва титриране на дозата. Лечението трябва да започне с въвеждането на 0,0625 mg (0,25 ml) подкожно през ден, като постепенно се увеличава дозата до 0,250 mg (1,0 ml), също прилагана през ден. Периодът на титриране на дозата може да бъде променен в случай на значима нежелана реакция. За постигане на достатъчна ефективност на терапията трябва да се прилага доза от 0,250 mg (1,0 ml) през ден.
Таблица за титриране на дозата:
В клинични проучвания продължителността на лечението при пациенти с пристъпно-ремитентна и вторично прогресираща множествена склероза е достигнала съответно 5 години и 3 години.
При пристъпно-ремитентна множествена склероза ефективността на лечението с Betaferon е демонстрирана през първите две години от лечението. Наличните данни за допълнителен 3-годишен период на лечение са в съответствие с данните за ефективността на лечението с Betaferon през целия период на лечение.
При пациенти с клинично изолиран синдром, предполагащ множествена склероза, прогресията на заболяването до CRMS е забавена с период от 5 години.
Лечението с Betaferon не се препоръчва при пациенти с пристъпно-ремитентна множествена склероза, които са имали по-малко от два пристъпа през последните 2 години, както и при пациенти с вторично прогресираща множествена склероза, които не са имали активна фаза на заболяването през последните 2 години.
Лечението с Betaferon трябва да се преустанови, ако пациентът не се повлияе от терапията, например, има стабилна прогресия на заболяването в рамките на 6 месеца по скалата EDSS (разширена скала за инвалидност) или, въпреки лечението с Betaferon, най-малко три курса от Необходима е терапия с АКТХ (адренокортикотропен хормон) или кортикостероиди за 1 година.
Приготвяне на инжекционен разтвор
А. Опаковка на лекарството, съдържаща флакони и предварително напълнени спринцовки:
За да разтворите лиофилизирания прах от интерферон бета-1b за инжектиране, използвайте предоставената готова спринцовка с разтворител и игла.
Б. Опаковка на лекарството, съдържаща флакони, предварително напълнени спринцовки, адаптер за флакон с игла и тампони със спирт:
За да разтворите лиофилизирания прах от интерферон бета-1b за инжектиране, използвайте предоставената готова спринцовка с разредител и адаптер за флакон с игла.
Във флакон с Betaferon се инжектират 1,2 ml разтворител (0,54% разтвор на натриев хлорид). Прахът трябва да се разтвори напълно, без да се разклаща. Преди употреба трябва да се провери готовият разтвор, който трябва да бъде от леко опалесциращ до опалесциращ, безцветен или светложълт. При наличие на частици или промяна в цвета на разтвора не трябва да се използва.
Неизползваният разтвор трябва да се изхвърли.
1 ml от приготвения разтвор съдържа 0,25 mg (8 милиона IU) интерферон бета-1b.
Необходимото количество от лекарството в съответствие с титрираната доза се изтегля в спринцовката след приготвяне на разтвора.
Техника на самоинжектиране на пациенти
За да приготвите своя собствена инжекция и инжекция Betaferon, моля, прочетете внимателно инструкциите и ги следвайте стъпка по стъпка. Лекарят или медицинската сестра ще ви запознаят с процедурата и техниката на самоинжектиране и ще ви помогнат да научите. Не се опитвайте да се инжектирате сами, докато не сте сигурни, че сте разбрали правилно изискванията за приготвяне на разтвора, както и техниката на самоинжектиране.
А. Опаковка на лекарството, съдържаща флакони и предварително напълнени спринцовки.
- Подготовка за инжектиране.
- Въвеждането на необходимия обем разтворител (1,2 ml) във флакона с Betaferon.
- Поставете необходимия обем инжекционен разтвор (1,0 ml) в спринцовка.
Подготовка за инжекция
1. Преди да поставите инжекция, вземете всичко необходимо за инжекцията.
За това ще ви трябва:
- напълнена спринцовка с Betaferon разредител (0,54% разтвор на натриев хлорид)
- флакон Betaferon
- игла 21G
- игла 30G
- спиртни кърпички
- контейнер за използвани спринцовки и игли
2. Измийте добре ръцете си със сапун.
3. Отстранете предпазната капачка от флакона Betaferon.
4. Избършете капачката на флакона Betaferon с тампон, напоен със спирт (избършете в една посока и използвайте една кърпа).
ЗАБЕЛЕЖКА: Оставете тампона със спирт върху капачката на флакона и не го отстранявайте, докато не сте готови да използвате флакона.
Въвеждането на необходимия обем от разтворителя (1,2 ml) във флакона с лекарството Betaferon
ЗАБЕЛЕЖКА: Вземете флакона Betaferon и изхвърлете тампона със спирт отгоре.
1. Като държите ръцете си на стабилна повърхност, извадете спринцовката с разтворител от опаковката. Издърпайте капачката, за да я отстраните от основата на спринцовката. Не докосвайте отворения връх на спринцовката. Не натискайте буталото.
2. Извадете иглата 21G от опаковката и я вкарайте здраво в върха на спринцовката. Отстранете предпазната капачка от иглата. Не докосвайте иглата.
3. Поставете флакона Betaferon върху стабилна повърхност, бавно вкарайте иглата на спринцовката (съдържаща 1,2 ml разтворител) докрай през запушалката на флакона.
4. Бавно натиснете надолу буталото. Иглата трябва да сочи настрани така
така че течността да тече надолу по стената на флакона (ако въведете разтворителя директно в
прах, тогава се образува много пяна).
5. Уверете се, че иглата не влиза в контакт с праха или получения продукт
решение.
6. Когато сте инжектирали цялото съдържание на спринцовката във флакона с Betaferon, дръжте флакона между палеца, показалеца и средния си пръст, така че иглата и спринцовката да са на ръката ви.
7. Внимателно завъртете флакона в ръката си, за да разтворите напълно праха Betaferon. НЕ РАЗТЪРСТВАЙТЕ!
8. Внимателно проверете разтвора (трябва да е прозрачен).
ЗАБЕЛЕЖКА: Ако сместа съдържа частици или е променила цвета си, излейте я и започнете цялата процедура отначало.
Комплект от необходимия обем инжекционен разтвор (1,0 ml) в спринцовка
ЗАБЕЛЕЖКА: Преди да изтеглите приготвения разтвор, натиснете напълно буталото на спринцовката, за да отстраните въздуха, който може да е останал вътре в спринцовката.
1. Наклонете леко флакона с Betaferon разтвор и поставете върха на иглата вътре
най-долната точка на флакона.
ЗАБЕЛЕЖКА: Не забравяйте да държите върха на иглата в разтвора през цялото време.
2. Издърпайте буталото и изтеглете 1,0 ml течност в спринцовката до маркировката.
3. Обърнете флакона с главата надолу и дръжте спринцовката с иглата нагоре.
4. Внимателно почукайте спринцовката, за да преместите въздушните мехурчета към горната част на цевта.
5. Внимателно натиснете надолу буталото, така че от спринцовката да излезе САМО ВЪЗДУХ.
6. Отделете спринцовката от иглата. Оставете иглата във флакона.
7. Поставете спринцовката (без иглата) върху равна повърхност. Уверете се, че върхът на спринцовката не докосва повърхността.
8. Вземете игла 30G, извадете я от опаковката и я поставете здраво на върха на спринцовката.
9. Изхвърлете бутилката с останалия разтвор и иглата.
Вече сте готови за инжектиране.
Б. Опаковка на лекарството, съдържаща флакони, предварително напълнени спринцовки, адаптер за флакон с игла и тампони със спирт.
Стъпки за приготвяне на разтвора:
1 - Измийте добре ръцете си със сапун, преди да започнете процедурата.
2 - Отворете бутилката с Betaferon - по-добре не с нокът, защото може да се счупи, а с палец - и я сложете на масата.

3 - Избършете капачката на флакона с тампон, напоен със спирт. Преместете кърпичката само в една посока и след това я оставете върху капачката на флакона.

4 - Отворете блистерната опаковка, съдържаща адаптера за флакона, но оставете адаптера вътре.
Не изваждайте адаптера за флакона от блистераопаковка.
Освен това внимавайте да не докоснете адаптера за флакона. Важно е да остане стерилен.

5 - Дръжте флакона на равна повърхност, докато прикрепяте адаптера.
6 - Отстранете тампона със спирт от капачката на флакона Betaferon. Поставете блистерната опаковка, съдържаща устройството за прехвърляне на разтвор с адаптер за флакон, върху капачката на флакона. Натиснете блистера с палец и показалец или длан, докато щракне.

7 - Хванете ръбовете на блистерната опаковка и я извадете от адаптера за флакона. Вече сте готови да прикрепите предварително напълнената спринцовка с разтворител към устройството за прехвърляне на разтвора.

8 - Вземете спринцовката. Завъртете оранжевата капачка на върха на спринцовката и я издърпайте от спринцовката. Изхвърлете капачката.

9 - Прикрепете спринцовката към отвора отстрани на адаптера, като поставите върха на спринцовката в него и внимателно я закрепете, като натискате, докато въртите по посока на часовниковата стрелка (както е показано със стрелката), за да оформите комплекта със спринцовката.

10 - Задръжте комплекта със спринцовката на дъното на флакона. Бавно натиснете буталото на спринцовката докрай надолу, за да преместите целия разредител във флакона. Освободете буталото. В този случай буталото може да се върне в първоначалното си положение.

11 - Направете няколко леки въртеливи движения с бутилката, така че сухият прах на Betaferon да се разтвори напълно. В този случай дизайнът със спринцовката остава все още прикрепен към флакона.
Не разклащайте флакона.

12 - Проверете внимателно разтвора. Тя трябва да е прозрачна и да не съдържа никакви частици. Ако
разтворът е променил цвета си или съдържа частици, излейте го и започнете цялата процедура отначало, като вземете нов пакет аксесоари. Ако се появи пяна - какво може да се случи, ако флаконът се разклати или
въртете твърде много - оставете бутилката да престои, докато пяната се утаи.
Подготовка на спринцовка

13 - Ако буталото се е върнало в първоначалното си положение, натиснете го отново и го фиксирайте. За да подготвите инжекцията, обърнете комплекта така, че флаконът да е отгоре и капачката на флакона да сочи надолу. Това ще позволи на разтвора да изтече в спринцовката.
Дръжте спринцовката хоризонтално.
Бавно дръпнете назад буталото, за да изтеглите целия разтвор от флакона в спринцовката.
14 - Завъртете комплекта спринцовка, така че иглата да сочи нагоре. Това ще доведе до издигане на въздушни мехурчета към повърхността на разтвора.

15 - Отстранете въздушните мехурчета, като леко потупате спринцовката и преместите буталото до маркировката 1 ml или повече.
количество, предписано от лекаря.
Ако във флакона е натиснат твърде много разтвор заедно с въздушни мехурчета, дръпнете буталото малко назад, за да изтеглите разтвора от флакона обратно в спринцовката. Направете това, докато целият въздух бъде отстранен и спринцовката съдържа 1 ml от приготвения разтвор.
Важна забележка: Когато събирате разтвора отново, върнете комплекта спринцовка в хоризонтално положение, при което флаконът е отгоре.

16 - След това хванете синия адаптер за флакон заедно с прикрепения към него флакон,
завъртете адаптера към вас и след това го отделете от спринцовката.
Когато отделяте адаптора за флакона от спринцовката, хващайте само синия пластмасов адаптер. Дръжте спринцовката в хоризонтално положение; флаконът трябва да е под спринцовката.

17 - В резултат на отделянето на флакона и адаптера от спринцовката, разтворът изтича от иглата по време на инжектирането.
18 - Вече сте готови да инжектирате.
ЗАБЕЛЕЖКА: Лекарството трябва да се приложи подкожно веднага след приготвянето на разтвора. Ако инжекцията се забави, разтворът трябва да се съхранява в хладилник и да се използва в рамките на 3 часа.Разтворът не трябва да се замразява.
19 - Изхвърлете флакона и останалия неизползван разтвор в контейнер за
отпадъци.
Кратко описание на подготовката на лекарството за инжектиране
1. Извадете съдържанието от опаковката.
2. Прикрепете адаптера за флакона към флакона.
3. Прикрепете спринцовката към адаптера за флакона.
4. Натиснете буталото, за да преместите разредителя във флакона.
5. Обърнете модула на спринцовката, след което издърпайте обратно буталото.
6. Отделете флакона от спринцовката - вече сте готови за инжектиране.
ЗАБЕЛЕЖКА: Лекарството трябва да се приложи подкожно веднага след приготвянето на разтвора. Ако инжекцията се забави, разтворът трябва да се съхранява в хладилник и да се използва в рамките на 3 часа.Разтворът не трябва да се замразява.
Избор и подготовка на мястото на инжектиране и приложение на лекарствения разтвор
Betaferon (1,0 ml) подкожно
- Избор на място за инжектиране
Бетаферон (интерферон бета-1b) трябва да се прилага подкожно. Меките места далеч от ставите и нервите са най-подходящи за това.
Местата за инжектиране могат да бъдат избрани с помощта на чертежа. Най-добре е първо да определите мястото на инжектиране и след това да подготвите спринцовката.
Ако ви е трудно да стигнете до някое място, помолете за помощ някой, който знае как да поставя инжекции.
1 - Изберете мястото на инжектиране (вижте фигурата "Редуващи се инжекции" в края на инструкциите).
ВАЖНА ЗАБЕЛЕЖКА: Не инжектирайте в области, където има неравности, подуване, твърди възли или болезненост. В допълнение, разтворът не трябва да се инжектира в онези области, където има промени в цвета на кожата, вдлъбнатини, корички или е нарушена целостта на кожата. Ако изпитвате тези или други необичайни състояния, свържете се с вашия доставчик на здравни услуги.
2 - Избършете кожата на мястото на инжектиране със спиртен тампон и оставете кожата да изсъхне на въздух. Изхвърлете салфетката.
Използвайте подходящ дезинфектант за дезинфекция на кожата.

3 - Отстранете предпазната капачка от иглата. Дръпнете капачката, вместо да я завъртате.
4 - Внимателно прищипете кожата около дезинфекцираната зона (за да я повдигнете малко).

5 - Вкарайте иглата направо в кожата под ъгъл от 90° с рязко, сигурно движение. Дръжте спринцовката като молив или
стрела.
6 - Бавно инжектирайте разтвора, като внимателно и непрекъснато натискате буталото. (Натиснете буталото докрай, докато спринцовката се изпразни).
7- Изхвърлете спринцовката в контейнер за отпадъци.
- Редуване на местата на инжектиране
Всеки път трябва да се избира ново място за инжектиране, тъй като редуването на местата за инжектиране позволява на кожата да заздравее и също така помага за предотвратяване на инфекция. По-добре е предварително да изберете мястото за инжектиране и едва след това да подготвите спринцовката. Схемата, показана на фигурата, ще ви помогне да редувате правилно местата на инжектиране. Например, ако сте направили първата инжекция в дясната половина на корема, след това направете втората в лявата половина, третата в дясното бедро и т.н. по схемата, докато не използвате всички възможни места за инжектиране. Запишете къде и кога последно сте инжектирали.


Следвайки предложената схема, след 8-та инжекция (след 16 дни) ще се върнете на мястото на първата инжекция (например дясната страна на корема). Това се нарича "цикъл на редуване". В нашата примерна диаграма всяка зона на свой ред е разделена на 6 места за инжектиране (за общо 48 места за инжектиране): отляво и отдясно, отгоре, в центъра и отдолу на съответната област. Когато след едно завъртане се върнете в една от зоните, изберете най-отдалеченото място на инжектиране в тази зона. Ако някоя област стане болезнена, обсъдете други възможни места за инжектиране с Вашия лекар.
Схема на преплитане:
За да ви помогнем да редувате правилно местата на инжектиране, се препоръчва да запишете кога и къде е поставена инжекцията. За да направите това, можете да използвате следната схема на разплитане:
1-ви цикълредуванеПървите 8 инжекции се правят последователно от 1-ва зона до 8-ма зона, като се използва само горният ляв сегмент на всяка зона.
2-ри цикълредуванеСледващите 8 инжекции започват отново от 1-ва зона, но те трябва да се направят в долния десен сегмент на всяка зона.
3-ти цикълредуванеСледващите 8 инжекции в този цикъл започват от 1-ва зона и се извършват последователно в централните леви сегменти на всяка зона.
Ако се следва тази последователност, всяка зона ще има възможност да се възстанови напълно преди следващата инжекция.
Регистрация на извършени инжекции
Инструкции за записване на местата и датите на извършените инжекции
Изберете място за инжектиране. Ако вече използвате Betaferon, тогава започнете със зоната, която не е била използвана по време на последния цикъл на редуване, т.е. през последните 16 дни.
След инжектиране запишете използваното място и датата на инжектиране (вижте фигурата „Пример за запис на извършени инжекции“ в края на инструкциите за употреба).


СТРАНИЧЕН ЕФЕКТ
Появата на нежелани реакции обикновено придружава започването на терапията. Честотата им намалява с времето.
Най-често може да се появи комплекс от грипоподобни симптоми (треска, втрисане, артралгия, общо неразположение, изпотяване, главоболие или миалгия) поради фармакологичното действие на лекарството Betaferon. Препоръчва се титриране на дозата в началото на лечението. Тежестта на грипоподобните симптоми може да бъде намалена чрез използване на нестероидни противовъзпалителни средства.
Често пациентите след въвеждането на лекарството Betaferon в доза от 0,25 mg (8 милиона IU) изпитват реакции на мястото на инжектиране (например зачервяване, подуване, обезцветяване на кожата, възпаление, болка, свръхчувствителност, некроза и не- специфични реакции).
Честотата на реакциите на мястото на инжектиране може да бъде намалена чрез използване на устройство за автоматично приложение на лекарството.
Нежеланите реакции (AR) при употребата на лекарството Betaferon, наблюдавани в хода на клиничните изпитвания и идентифицирани в процеса на следрегистрационно наблюдение, и честотата на тяхната поява са представени по-долу.
Най-подходящият термин от Медицинския речник за регулаторни дейности (MedDRA) се използва за описание на специфичната реакция, нейните синоними и свързаните с нея състояния.
Маса 1: Нежелани събития и отклонения на лабораторните показатели, наблюдавани при клинични изпитвания с честота на поява ≥ 10% и синдром, включващ поне две от следните нежелани реакции:
треска, втрисане, миалгия, неразположение и изпотяване;
3 - отклонение от нормата на лабораторните параметри;
4
Betaferon при пациенти с клинично изолиран синдром, което позволява
предполагат множествена склероза, p< 0,05;
5
- нежелани събития, до голяма степен свързани с употребата на лекарството
Betaferon при пациенти с пристъпно-ремитентна множествена склероза,
стр< 0,05;
6
- нежелани събития, до голяма степен свързани с употребата на лекарството
Betaferon при пациенти с вторично прогресираща множествена склероза, стр< 0,05;
7
- не са наблюдавани промени в профила по време на клиничното проучване BENEFIT
безопасност на Betaferon.
Таблица 2: Нежеланите реакции, идентифицирани по време на следрегистрационните наблюдения и за които е установена честотата на поява, се определят въз основа на сборни данни от клинични проучвания (
3 - отнася се за всички препарати, съдържащи интерферон (вижте следното
