pH vodenih rastvora mlečne kiseline. Mliječna kiselina (2-hidroksipropionska kiselina)
MLIJEČNA KISELINA(2-hidroksipropionska kiselina) CH 3 CH(OH)COOH, molekulska težina 90,1; bezbojni kristali. Poznata D(+)-mliječna kiselina, D(-)-mliječna (mesno-mliječna) kiselina i racemična. MLIJEČNA KISELINA.-mliječna kisela fermentacija. Za D,L- i D-M.k. tačka topljenja 18 °C i 53 °C; tačka ključanja, respektivno, 85 ° C / 1 mm Hg. i 103°C/2mm Hg; za D-M.k. [a] D 20 -2,26 (koncentracija 1,24% u vodi). Za D,L-M. K. DH 0 arr - 682,45 kJ / mol; DH 0 pl 11,35 kJ/mol; DH test 110,95 kJ/mol (25°C), 65,73 kJ/mol (150°C). Za L-M.k. DH 0 spaljen - 1344,8 kJ/mol; DH 0 arr -694,54 kJ/mol; DH 0 pl 16,87 kJ/mol.
Zbog visoke higroskopnosti MLEČNE KISELINE. obično koriste njegov koncentrator. vodeni rastvori, sirupasti, bezbojni. tečnosti bez mirisa. Za vodene otopine MLIJEČNA KISELINA. d 20 4 1,0959 (40%), 1,1883 (80%), 1,2246 (100%); n D 25 1,3718 (37,3%), 1,4244 (88,6%); h 3,09 i 28,5 MPa. s (25 0 C), respektivno, za 45,48 i 85,32% rastvora; g 46.0. 10 -3 N/m (25°C) za 1 M rastvor; e 22 (17°C). MLEČNA KISELINA rastvorljiv u vodi, etanolu, slabo u benzenu, hloroformu i drugim halougljicima; pKa 3,862 (25°C); pH vodenih rastvora 1,23 (37,3%), 0,2 (84,0%).
Oksidacija MLIJEČNA KISELINA. obično praćeno razgradnjom. Pod dejstvom HNO 3 ili O 2 nastaju vazduh u prisustvu Cu ili Fe, HCOOH, CH 3 COOH, (COOH) 2, CH 3 CHO, CO 2 i pirogrožđana kiselina. Oporavak MLIJEČNA KISELINA. HI dovodi do propionske kiseline, a smanjenje prisustva Re black dovodi do propilen glikola.
M. do. dehidrira do akrilne kiseline, kada se zagreva sa HBr formira 2-bromopropionsku kiselinu, kada Ca-sol reaguje sa PCl 5 ili SOCl 2 -2-hloropropionil hloridom. U prisustvu mineralne kiseline dolazi do samoesterifikacije MLEČNA KISELINA. sa formiranjem laktona formule I, kao i linearnih poliestera. Kod interakcije MLIJEČNA KISELINA. sa alkoholima nastaju hidroksi kiseline RCH 2 CH(OH)COOH, a interakcijom soli MLEČNA KISELINA. sa alkoholima i etrima. Soli i estri MLIJEČNE KISELINE nazivaju se laktati (vidi tabelu).
M.k. nastala kao rezultat fermentacija mliječne kiseline(pri kiseljenju mlijeka, kiselog kupusa, kiseljenja povrća, zrenja sira, siliranja stočne hrane); D-M.k. nalazi se u tkivima životinja, biljaka, kao i u mikroorganizmima.
MLEČNA KISELINA se u industriji dobija hidrolizom 2-hloropropionske kiseline i njenih soli (100°C) ili laktonitrila CH 3 CH (OH) CN (100° C, H 2 SO 4) nakon čega sledi formiranje estera, izolovanje i čija hidroliza dovodi do proizvoda Visoka kvaliteta. Postoje i druge metode za dobijanje MLEČNE KISELINE: oksidacija propilena sa azotnim oksidima (15-20°C) nakon čega sledi tretman sa H 2 SO 4, interakcija CH 3 CHO sa CO (200° C, 20 MPa).
SVOJSTVA NEKIH LAKTATA
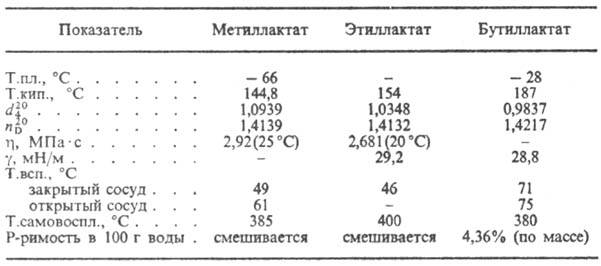
M.k. koristi se u prehrambenoj industriji, u farbanju, u industriji kože, u fermentacionim radnjama kao baktericidno sredstvo, za dobijanje leka. sri, plastifikatori. Etil i butil laktati se koriste kao rastvarači za celulozne etere, ulja za sušenje i uzgoj. ulja; butil laktat - također kao otapalo za neke sintetičke. polimeri.
Svjetska proizvodnja MLIJEČNA KISELINA. 40 hiljada tona (1983).
Hemijska enciklopedija. Sveska 3 >>
Racionalna nomenklatura enzima se sastavlja tako što se latinskom korijenu naziva supstrata na koji enzim djeluje, ili nazivu procesa koji enzim katalizira, dodaje završetak "aza".
Na primjer, enzim koji djeluje na škrob (amilum) naziva se amilaza; urea (urea) - ureaza; fenola - fenolaze itd.
Pored racionalnog naziva, sačuvani su i ranije pojavljivani termini: pepsin, tripsin.
1961. godine, novi međunarodna klasifikacija, na osnovu tipa katalizirane reakcije.
Trenutno je poznato oko 3000 različitih enzima. Klasificirani su prema vrsti djelovanja. Postoji 6 klasa enzima:
1 .Oksidoreduktaza – redoks
enzimi; katalizuju biološku oksidaciju.
2.Transferaze - kataliziraju prijenosne reakcije raznih hemijske grupe od jednog molekula (donora) do drugog molekula (akceptora).
3. Hidrolaze - vrše hemijske transformacije supstanci uz učešće molekula vode.
4. Liase - odcijepiti jednu ili drugu grupu od supstrata nehidrolitičkim putem.
5. Izomeraze - izvršiti izomerne transformacije jedinjenja.
6. ligaze (sintetaze) - katalizuju reakcije sinteze, praćene eliminacijom fosforne kiseline iz ATP-a ili drugog trifosfata.
I klasa. Oksidoreduktaza su enzimi redoks reakcija koje leže u osnovi biološka oksidacija. Naziv enzima sastavljen je u sljedećem obliku: naziv supstrata (donora) od kojeg se odvajaju atomi vodika (elektroni), naziv akceptora na koji se prenose atomi vodika i završava se nazivom "oksidoreduktaza": na primjer, laktat: NAD-oksidoreduktaza.
Razlikuju se sljedeće podklase:
1) aerobne dehidrogenaze koje prenose elektrone i protone vodika sa oksidiranog supstrata na kisik:
H 2 S + O 2 S oksidirani + H 2 O 2
hidrogen sulfid
to uključuje enzime oksidaze;
2) anaerobne dehidrogenaze prenose elektrone i protone vodonika sa oksidiranog na drugi supstrat. To uključuje dehidrogenaze zavisne o piridinu i flavinu. Na primjer, oksidacija mliječne kiseline nastaje pod djelovanjem laktat dehidrogenaze, dok se NAD reducira u NADH 2:

mlečna kiselina pirogrožđana kiselina
Oksidacija jantarne kiseline nastaje pod dejstvom sukcinat dehidrogenaze, dok se FAD redukuje u FADH 2.

jantarna kiselina fumarna kiselina
3) transportaze elektrona - prenosioci elektrona. To uključuje enzime citokroma, citokrom oksidaze mitohondrijalnog respiratornog lanca
4) peroksidaza i katalaza. Peroksidaza katalizira oksidaciju supstrata vodikovim peroksidom. Na primjer, pod djelovanjem peroksidaze, sumporovodik se oksidira uz sudjelovanje vodikovog peroksida:
H 2 S + H 2 O 2 S oksidirani + 2H 2 O
Katalaza kod životinja razlaže vodikov peroksid na vodu i molekularni kiseonik:
2H 2 O 2 2H 2 O + O 2
Katalaza neutralizira djelovanje peroksida i izvor je molekularnog kisika u tkivima.
II razred. Transferaze- kataliziraju reakcije prijenosa atoma i grupa atoma, uključuju sljedeće podklase:
1) Aminoferaze su enzimi koji prenose amino grupe iz jedne supstance u drugu. Koenzim je derivat vitamina B 6 (piridoksina): na primjer, glutaminska kiselina donira amino grupu piruvatu, kao rezultat toga, sintetizira se alanin i nastaje a-ketoglutarna kiselina.

glutamin piruvat α - ketoglutarni alanin
kisela kiselina
Piridoksin, enzim koji izvodi ovu reakciju, naziva se 1-glutamil:piruvat aminotransferaza ili, prema staroj nomenklaturi, aminoferaza.
2) Aciltransferaze - ubrzavaju transfer acila (ostataka karboksilne kiseline) u aminokiseline, alkohole i druga jedinjenja. Na primjer, sinteza acetilholina se provodi uz sudjelovanje enzima kolin acetiltransferaze:

3) Fosfotransferaze - enzimi koji ubrzavaju reakciju prenošenja ostatka fosforne kiseline. Najčešći donor fosfatnih ostataka je ATP. Na primjer, heksokinaza ubrzava prijenos ostataka fosforne kiseline na glukozu:

α-D-glukoza glukoza-6-fosfat
4) Metilferaze - enzimi koji prenose metil grupu s jednog spoja na drugo: na primjer, u sintezi kreatina, metionin je donor metil grupe.
5) Glukoziltransferaze - nosioci glukozida
ostaci:
11 (C 6 H 12 O 6) + UDP - glukoza (n + 1) (C 6 H 12 O 6) + UDP
tu spadaju glikogen sintaze, glukoziltransferaze, fosforiboziltransferaze, itd.
6) Alkiltransferaze - nosioci alkoholnih ostataka. To uključuje holin transferazu, fosfatildietanolamin transferazu, itd.
III razred. Hidrolaze- razbiti unutarmolekulske veze dodavanjem elemenata vode:
R - R 1 + HOH R - H + R 1 - OH
To uključuje sljedeće podklase:
1) Esteraze - enzimi koji hidroliziraju esterske veze prema shemi:
R 1 -0-R 2 + HOH R 1 -H + R 2 -OH
Na primjer, fosfodiesteraze - hidroliziraju estere fosfora:
Diacilglicerol 3-fosforna kiselina + HOH diacilglicerol + H 3 PO 4.
Ova podklasa uključuje: fosfataze (kisele, alkalne), glukoza-6-glukoza-1-fosfatazu, RNKazu, itd.
Karboksiesteraze - hidrolizuju estarske veze:

tristearin glicerin stearinska
Ovi enzimi uključuju lipaze, lecitinaze, jednostavne esteraze itd.
Sulfoesteraze - hidroliziraju sulfatne estere prema sljedećoj shemi:
fenol sumporna kiselina fenol sumporna kiselina
2) Glikozidaze - hidroliziraju glikozidne veze, tu spadaju α- i β-amilaze, maltaza, laktaza, saharaza.
3) Peptidaze. Postoje endopeptidaze - pepsin, tripsin, hemotripsin; egzopeptidaze - aminopeptidaze, karboksipeptidaze, dipeptidaze, tripeptidaze.
Peptidaze hidroliziraju peptidne veze sljedećom reakcijom:
![]()
alanilalanin alanin
Kao rezultat hidrolize nastaju dva molekula alanina.
4) Amidaze - enzimi koji hidroliziraju amidne veze purinskih i pirimidinskih baza, amida aminokiselina i
arginin. primjeri:
A) Adenin + H 2 O hipoksantin + NH 3
purin deaminaza

glutamin glutamin

arginin urea ornitin
5) Polifosfataze - hidroliziraju veze fosfornog anhidrida:
ATP + H 2 O ADP + H 3 PO 4
Ova grupa uključuje Na + , K + , Mg 2+ -ATPazu, itd.
IV razred. Liaze su enzimi koji cijepaju veze bez sudjelovanja vode, a pritom se raskidaju C-C konekcije, C-N obveznice, C-O veze. To uključuje enzime aldolaze, dekarboksilaze i druge. Na primjer, aldolaza razbija C-C veze heksoze (1,6-difosfofruktoze) kako bi se formirale dvije trioze, fosfodioksiaceton i fosfogliceraldehid:

V klasa. Izomeraze: kataliziraju izomerizaciju, izomernu transformaciju molekula, kao što je glukoza u fruktozu. Mutaze mijenjaju lokaciju različitih grupa ili atoma u molekulu. Tu spadaju: fosfogliceromutaza, fosfoglukomutaza, fosfofruktomutaza itd. Na primjer, fosfodioksiaceton se pretvara izomerazom u fosfogliceraldehid:

fosfodioksiaceton fosfogliceraldehid
VI razred. Ligaze (sintetaze) su enzimi koji kataliziraju vezivanje molekula jedan za drugi. Na primjer:
Aminokiselina + tRNA aminoacil-tRNA
To uključuje enzime: DNK polimeraze, RNA polimeraze, enzime koji kataliziraju sintezu proteina, itd.
reagensi:
Ftalna kiselina
napredak:
~0,1-0,2 g ortoftalne kiseline stavi se u suhu epruvetu i zagreje na plamenu alkoholne lampe, držeći epruvetu horizontalno. Formira se ftalni anhidrid koji sublimira i ponovo kondenzuje na hladnim zidovima epruvete. Epruveta se hladi, zatim se talog ftalnog anhidrida pažljivo zagreva, lako se topi i spušta na dno epruvete.
Iskustvo br. 56. Dobijanje fenolftaleina
reagensi:
Ftalni anhidrid
napredak:
~ 0,2 g fenola, ~ 0,1 g ftalnog anhidrida, ~ 5 kapi koncentrovane sumporne kiseline stavi se u suvu epruvetu i lagano zagreje na plamenu alkoholne lampe. Smjesa se topi, fenol kondenzira s ftalnim anhidridom:

Zatim se cijev hladi na zraku. U ohlađenu smjesu dodajte pola epruvete vode i snažno protresite. Dobijeni rastvor se prebacuje u drugu epruvetu i dodaje se nekoliko kapi rastvora alkalije. U alkalnom okruženju pojavljuje se grimizno-crvena boja, što ukazuje na prisustvo fenolftaleina u otopini.
U alkalnoj sredini dolazi do izomerizacije jedne od jezgri benzena, formira se hinoidna grupa koja uzrokuje pojavu boje. Kada se rastvor zakiseli, boja nestaje, a kada se doda lužina, ponovo se pojavljuje. Specificirano svojstvo fenolftaleina koristi se u analitičkoj hemiji kao indikator (indikator) reakcije medija.
Ako umjesto fenola uzmemo resorcinol (dihidrični fenol) i izvršimo eksperiment na isti način kao što je gore opisano, tada nastaje fluorescein. Rastvor fluoresceina u alkalnom mediju ima lijepu boju, crvenu u propuštenoj svjetlosti, zelenu u reflektiranoj svjetlosti (fluorescencija).
VIII. HIDROKSIJACIDE
Iskustvo br. 57. Detekcija mliječne kiseline
reagensi:
Rastvor 1% fenola
Otopina 1% željeznog hlorida
Mliječna kiselina
napredak:
U ~3 ml 1% rastvora fenola dodajte nekoliko kapi 1% rastvora gvožđe (III) hlorida. Tečnost postaje svijetlo ljubičasta zbog stvaranja složenih fenolata željeza. U nastalu tečnost dodaje se nekoliko kapi mliječne kiseline i boja otopine mijenja se u zeleno-žutu zbog stvaranja željeznog laktata (CH 3 CH (OH) COO) 3 Fe.
Iskustvo br. 58. Razgradnja mliječne kiseline zagrijavanjem s koncentriranom sumpornom kiselinom
reagensi:
Mliječna kiselina
koncentrovane sumporne kiseline
napredak:
Mješavina jednakih volumena (~0,5 ml svaki) mliječne i sumporne kiseline pažljivo se zagrijava u epruveti sa epruvetom za izlaz plina. Oslobođeni ugljični monoksid (II) se pali na otvoru cijevi za izlaz plina, gori plavkastim plamenom.
- α-hidroksipropionska (2-hidroksipropanska) kiselina, CH 3 CH(OH)COOH. Jednobazna hidroksikarboksilna kiselina; važan metabolički međuprodukt kod životinja, biljaka i mikroorganizama; ograničavajuća monokarboksilna kiselina acikličkog niza

Otkrio ga je švedski hemičar Carl Scheele 1780.
Godine 1807. Jens Jakob Berzelius izolirao je cinkovu sol mliječne kiseline iz mišića.
Opis i svojstva
Bezbojni kristali, lako rastvorljivi u vodi, etanolu, slabo - u benzenu, hloroformu. Postoji u dva optički aktivna (-)- i (+)-oblika ( t pl 25-26 °C) iu obliku neaktivnog racemskog (±)-forma (t pl 18 °C).
Reakcije

Mliječna kiselina kod ljudi i životinja
Mliječna kiselina nastaje razgradnjom glukoze. Ponekad se naziva "šećerom u krvi", glukoza je glavni izvor ugljikohidrata u našem tijelu. To je glavno gorivo za mozak i nervni sistem, kao i za mišiće tokom vježbanja. Kada se glukoza razgradi, stanice proizvode ATP (adenozin trifosfat), koji osigurava energiju za većinu hemijske reakcije u organizmu. Nivo ATP-a određuje koliko brzo i koliko dugo se naši mišići mogu kontrahirati kada fizička aktivnost. Za proizvodnju mliječne kiseline nije potrebno prisustvo kisika, zbog čega se ovaj proces često naziva "anaerobni metabolizam". Mnogi ljudi vjeruju da mišići proizvode mliječnu kiselinu kada ne dobiju dovoljno kisika iz krvi. Drugim riječima, vi ste u anaerobnom stanju. Međutim, naučnici tvrde da se mlečna kiselina formira i u mišićima koji primaju dovoljno kiseonika. Povećanje količine mliječne kiseline u krvotoku samo ukazuje na to da nivo njenog unosa premašuje nivo uklanjanja. Kiseonik ovde ne igra značajnu ulogu. Proizvodnja ATP-a zavisna od laktata je vrlo mala, ali ima visoku stopu. Ova okolnost ga čini idealnim za upotrebu kao gorivo kada opterećenje prelazi 50% maksimalnog. Tokom odmora i submaksimalnog (prilično umjerenog, submaksimalno se obično podrazumijeva 90% maksimalnog) opterećenja, tijelo radije razgrađuje masti za energiju. Pri opterećenjima od 50% od maksimuma (prag intenziteta za većinu programa treninga), tijelo se ponovo gradi na preferencijalnu potrošnju ugljikohidrata. Što više ugljikohidrata koristite kao gorivo, to više više proizvodnje mlečne kiseline.
Da bi se omogućilo prolaz glukoze ćelijske membrane Treba joj insulin. Molekula mliječne kiseline je upola manja od molekule glukoze i ne treba joj hormonsku potporu – lako sama prolazi kroz ćelijske membrane.
Aplikacija.
Mlečna kiselina se koristi u prehrambenoj industriji, u farbanju, u industriji kože, u fermentacionim radnjama kao baktericidno sredstvo, za dobijanje lijekovi, plastifikatori. Etil i butil laktati se koriste kao rastvarači celuloznih etera, ulja za sušenje, biljna ulja; butil laktat - također se koristi kao rastvarač za neke sintetičke polimere.
Svjetska proizvodnja mliječne kiseline - 40 hiljada tona (1983).
 Heinrich Otto Wieland
Heinrich Otto Wieland
 Adolf Johann Friedrich Wilhelm von Bayer
Adolf Johann Friedrich Wilhelm von Bayer
 Friedrich Bergius
Friedrich Bergius  opšte karakteristike metali. Pojava u prirodi i rasprostranjenost. Metode dobijanja i čišćenja
opšte karakteristike metali. Pojava u prirodi i rasprostranjenost. Metode dobijanja i čišćenja
 Krom kao hemijski element
Krom kao hemijski element
Stranica 1
Oksidacija mliječne kiseline olovnim dioksidom dovodi do stvaranja acetaldehida.
Kada se mliječna kiselina oksidira kalij-dihromatom u prisustvu sumporne kiseline, nastaje acetaldehid koji se hvata destilacijom s Nesslerovim reagensom. Boja potonjeg ukazuje samo na moguće prisustvo mliječne kiseline u uzorku.
Zadatak 10.7. Oksidacija mliječne kiseline u poligradnu (2-oksopropansku) kiselinu javlja se u živim organizmima kao jedna od faza biološkog odmrzavanja ugljikohidrata.
Pirogrožđana kiselina se može sintetizirati oksidacijom mliječne kiseline (vidjeti sek.
Energija koja se oslobađa tokom oksidacije mliječne kiseline koristi se u mišićima za resintezu glikogena.
Primjer ove reakcije je oksidacija mliječne kiseline u pirogrožđanu kiselinu.
Detaljno smo proučavali uticaj kiselosti sredine i viška oksidacionog agensa pri oksidaciji mliječne kiseline kalijevim bihromatom.
Ako se mišić zatrovan proizvodom vlastite vitalne aktivnosti prenese u atmosferu kisika, tada se slika mijenja. Počinju dva procesa: oksidacija mliječne kiseline, što rezultira dodatnim i vrlo značajnim oslobađanjem energije, i sinteza glikogena. Pokazalo se da su procesi postupne konverzije glikogena u glukozu, a zatim u mliječnu kiselinu reverzibilni u svim svojim najvažnijim fazama. Biohemijska mašina može raditi unazad i ponovo stvarati sirovine iz finalnih proizvoda. Neki dio mliječne kiseline – krajnjeg produkta glikogenolize (razgradnje glikogena) ponovo prelazi u sirovinu – glikogen.
Metoda se zasniva na mjerenju intenziteta boje spoja koji nastaje u reakciji cetaldehida, koji je nastao oksidacijom mliječne kiseline paraoksidifenilom.
Iako citokrom b2 katalizira razgradnju drugih supstrata (a-hidroksi-n-butirata, a-hidroksi-m-kaproata, oc-hidroksiizokaproata), njihova koncentracija u biološkim medijima je nekoliko redova veličine niža od koncentracije mliječne kiseline, pa je ometajući efekat je zanemarljivo mali. Veliki broj metabolita sa redukcijskim svojstvima, na primjer mokraćne kiseline, glutation, cistein, adrenalin, vitamin C, p-alanin, oksidiraju se ili [Fe (CN) 6 ] 3, ili na platinskoj elektrodi, a njihova oksidaciona struja se dodaje struji koja odgovara oksidaciji mliječne kiseline. Stoga je u prisustvu ovih metabolita nepoželjno provoditi određivanje mliječne kiseline.
Takav aparat je opisan za mikroodređivanje treonina pomoću t-hidroksidifenila (vidi poglavlje Oksidacija mliječne kiseline u acetaldehid se završava na 50 vodenom kupatilu u trajanju od 30 minuta. Za isto vrijeme, acetaldehid se uduvava u 15 ml jakog HtaSCh koji sadrži višak n-oksidifenila.Cijela operacija izvedena kao što je opisano u pogl.
Epruvete sa filtratom stavljaju se u ledenu vodu i polako, kap po kap, dodaju 1 ml koncentrovane sumporne kiseline. Epruvete treba lagano protresti cijelo vrijeme i osigurati da se njihov sadržaj ne zagrije. Kako bi se ubrzala oksidacija mliječne kiseline, obje epruvete se premeštaju u kipuću kupku na 4 minute, a zatim se brzo hlade u ledenoj vodi. Nakon hlađenja, dodajte 1 - 2 kapi 0 1% rastvora veratrola u svaku epruvetu, lagano protresite nekoliko minuta. U eksperimentalnom uzorku razvija se svijetlo ružičasta boja, jer je do glikolize došlo pod utjecajem enzima mišićnog tkiva. U kontrolnom uzorku, boja je blago ružičasta zbog mliječne kiseline koja je prije početka eksperimenta bila prisutna u mišićnoj pulpi.
Lurijina grupa je pokazala da vezivanje proteinskih molekula kolicina K i E1 za ćelije bakterije E-coli prati prestanak sinteze makromolekula: proteina, DNK, RNK i glikogena. Aktivan transport mlečnog šećera (laktoze), glutamina, razne aminokiseline i joni kalijuma i magnezijuma. U isto vrijeme, stanica nastavlja akumulirati glukozu, čiji se aktivni transport osigurava direktno energijom oksidacije mliječne kiseline.
Također je jedan od međuproizvoda u mliječnoj kiselini i alkoholna fermentacija ugljikohidrati. Može se dobiti interakcijom acetil hlorida sa kalijum cijanidom, nakon čega sledi hidroliza nastalog ketononitrila, ili oksidacija mliječne kiseline.
Reakcija se izvodi sa filtratima u prisustvu mliječne kiseline. Da biste to učinili, uzmite 2 čiste numerisane epruvete: u prvoj - 10 kapi filtrata kontrolni uzorak, u drugom - 10 kapi filtrata eksperimentalnog uzorka. Ne smijemo zaboraviti da jako pregrijavanje može dovesti do ugljenisanja mliječne kiseline. Da bi se ubrzala oksidacija mliječne kiseline, obje epruvete se premeštaju u kipuću vodenu kupelj na 4-5 minuta, a zatim se brzo hlade u ledenoj vodi. Dodajte 3 kapi 0 2% alkoholnog rastvora veratrola ili gvajakola u svaku epruvetu u ohlađene tečnosti.
