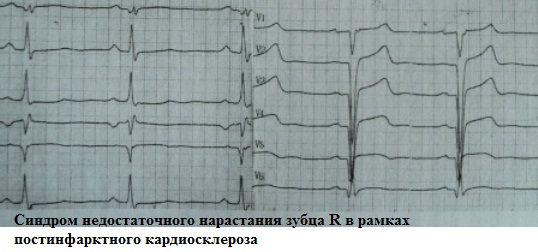
Caratteristiche della diagnostica elettrocardiografica nelle persone di età più avanzata. Onda R lenta Segni di pseudo-infarto con sovraccarico dei ventricoli del cuore Crescita insufficiente dell'onda r in v1 v2
Fai un test online (esame) su questo argomento ...
Onda R(di base Onda ECG) è dovuto all'eccitazione dei ventricoli del cuore (per maggiori dettagli, vedere "Eccitazione nel miocardio"). L'ampiezza dell'onda R nelle derivazioni standard e potenziate dipende dalla posizione asse elettrico cuore (e.o.s.). Con una posizione normale dell'e.o.s. R II > R I > R III .


- L'onda R può essere assente nell'aVR con piombo potenziato;
- Con una disposizione verticale dell'e.o.s. L'onda R può essere assente nella derivazione aVL (sull'ECG a destra);
- Normale ampiezza dell'onda R in piombo aVF più che dentro piombo standard III;
- IN cavi del torace L'ampiezza dell'onda R V1-V4 dovrebbe aumentare: R V4 > R V3 > R V2 > R V1 ;
- Normalmente, l'onda r può essere assente nella derivazione V1;
- Nei giovani, l'onda R può essere assente nelle derivazioni V1, V2 (nei bambini: V1, V2, V3). Tuttavia, un tale ECG è spesso un segno di infarto miocardico anteriore. setto interventricolare cuori.
Fai un test online (esame) su questo argomento ...
ATTENZIONE! Informazioni fornite dal sito sito web ha carattere referenziale. L'amministrazione del sito non è responsabile per eventuali Conseguenze negative in caso di assunzione di farmaci o procedure senza prescrizione medica!
Ospedale clinico FKUZ MSCh MIA RF a MoscaCentro consultivo e diagnostico n. 6, Mosca
nel reparto di terapia intensiva e terapia intensiva ha osservato un paziente con insufficienza cardiaca cronica, fibrillazione atriale e alterazioni dell'elettrocardiogramma, che potrebbero essere causati sia dalla cardiosclerosi postinfartuale sia dal posizionamento improprio degli elettrodi o dalla destrocardia.
Parole chiave: destrocardia, ECG, scompenso cardiaco, case report.
In primo luogo ha identificato la destrocardia e la complessità associata della diagnostica presso l'unità di terapia intensiva
AV Syrov
Ospedale clinico per gli affari interni di Mosca
Centro consultivo e diagnostico №6, Mosca
Il documento descrive il caso avvenuto presso il pronto soccorso e terapia intensiva. Paziente con insufficienza cardiaca cronica, fibrillazione atriale presentava alterazioni specifiche dell'elettrocardiogramma, che potrebbero essere state causate da cardiosclerosi post-infartuale, errata applicazione degli elettrodi o destrocardia.
parole chiave: destrocardia, ECG, scompenso cardiaco, case report.
Il paziente M., 91 anni, è stato ricoverato in terapia intensiva con grave mancanza di respiro, tosse secca. Al momento del ricovero, mancanza di respiro 28 movimenti respiratori al minuto Rantoli umidi nelle parti inferiori dei polmoni su entrambi i lati. Pressione sanguigna 180/105 mm Hg. Art., frequenza cardiaca 85-115 battiti / min. Fibrillazione atriale. Storia forma permanente fibrillazione atriale, ipertensione perenne. Si nota ovunque un aumento della dispnea L'anno scorso. Entro un mese, c'è stato un forte aumento della mancanza di respiro, la comparsa di una tosse secca.
Diagnosi preliminare: cardiopatia ischemica. Fibrillazione atriale, forma permanente. Malattia ipertonica 3 art. Cuore ipertonico. Scompenso acuto dell'insufficienza cardiaca cronica.
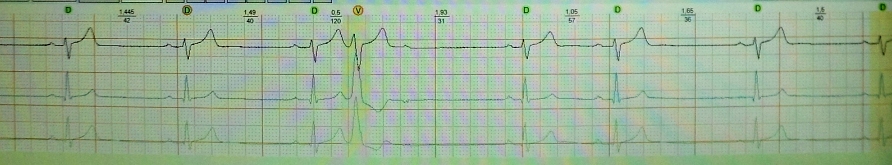
Il primo elettrocardiogramma (ECG) ha rivelato fibrillazione atriale, onde Q nelle derivazioni I, II, AVL, AVF, V2-V6 (Fig. 1).
Con un precedente infarto miocardico sull'ECG, il cambiamento più indicativo è la presenza di onde Q patologiche.L'onda Q è considerata patologica se la sua larghezza è pari o superiore a 0,04 s e la profondità è almeno il 25% dell'ampiezza della R onda nello stesso vantaggio. Tuttavia, l'assenza di onde R in quasi tutte le derivazioni non è tipica dei cambiamenti postinfartuali, che di solito sono locali.
Se l'ECG non esclude la cardiosclerosi postinfartuale, allora uno studio ecocardiografico aiuta a valutare funzione contrattile ventricolo sinistro. La violazione della contrattilità locale e una diminuzione della frazione di eiezione del ventricolo sinistro confermano la presenza di cardiosclerosi postinfartuale.
Il posizionamento errato degli elettrodi sugli arti è facilmente determinabile dall'elettrocatetere aVR. Le onde P e T in questa derivazione dovrebbero essere negative e complesso QRS opposto al complesso QRS nella derivazione II. In questo caso, il rapimento aVR soddisfa pienamente i criteri sopra descritti e ci consente di escludere posizione sbagliata elettrodi.
Con la destrocardia, il cuore si trova nella metà destra del mediastino, rispecchiando la posizione normale. L'ECG mostra una configurazione inversa in entrambe le derivazioni degli arti e del torace. Quando le derivazioni del torace vengono applicate a destra dello sterno, in un'immagine speculare della posizione abituale degli elettrodi del torace e della posizione inversa delle derivazioni dagli arti, l'ECG assume la sua forma abituale.
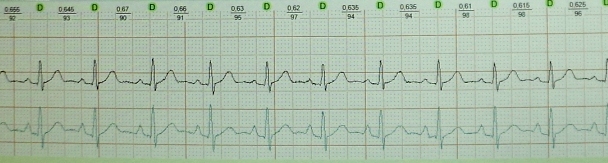
Quando l'ECG è stato ripreso utilizzando la tecnica sopra descritta (disposizione degli elettrodi invertita, Fig. 2), le onde R sono apparse nelle derivazioni I, II, AVL, AVF, V5-V6 e un'onda r è apparsa nelle derivazioni V2-V4. Il secondo ECG mostra fibrillazione atriale e blocco della ramificazione antero-superiore del ramo sinistro del fascio di His e crescita insufficiente delle onde R nelle derivazioni toraciche (l'ampiezza delle onde R nelle derivazioni V1-V3 non supera i 3 mm, il l'ampiezza dell'onda R in V3 è maggiore dell'onda R in V2). Maggior parte causa comune la crescita insufficiente dell'onda R è l'ipertrofia ventricolare sinistra, tuttavia, non è possibile escludere completamente la cardiosclerosi postinfartuale mediante ECG.
L'ecocardiografia ha rivelato destrocardia. Non sono state rilevate violazioni della contrattilità locale del miocardio. Il ventricolo sinistro è ipertrofico (lo spessore del setto interventricolare è di 16 mm, parete posteriore- 15 mm), la funzione sistolica è preservata (frazione di eiezione 55% secondo Simpson), la funzione diastolica è compromessa. È stata rilevata dilatazione atriale.
A esame ecograficoè stata anche rivelata la destroposizione degli organi addominali.
Così, le modifiche iniziali dell'ECG che si sono verificate erano dovute alla destrocardia. La crescita insufficiente delle onde R nelle derivazioni toraciche non è dovuta a cambiamenti cicatriziali, ma all'ipertrofia ventricolare sinistra. L'aumento della mancanza di respiro era dovuto all'insufficienza cardiaca cronica, confermata da un aumento del peptide natriuretico cerebrale a 5 mila ng/l. La causa di CHF era una violazione della funzione diastolica del ventricolo sinistro (insufficienza cardiaca diastolica), ipertensione arteriosa e fibrillazione atriale.
L'ospedale è stato prescritto trattamento successivo: ACE-inibitore(fosinopril 20 mg 2 volte al giorno), beta-bloccante (metoprololo succinato 50 mg 1 volta al giorno), diuretici (veroshpiron 50 mg 1 volta al giorno, furosemide 20 mg per via endovenosa, quindi 20 mg per via orale 1 volta al giorno per breve periodo), un anticoagulante (warfarin con un INR target di 2,0-3,0; la dose iniziale del farmaco è di 5 mg 1 volta al giorno, la dose di mantenimento è di 3,75 mg 1 volta al giorno), una statina (atorvastatina 20 mg / die) . Il paziente è stato dimesso in condizioni soddisfacenti. Mancanza di respiro con normale attività fisica non è stato osservato. Normosistolia, frequenza cardiaca 70-85 battiti / min, pressione arteriosa 120–135/70–65 mmHg Arte.
È comune un piccolo guadagno dell'onda R Sintomo ECG, che è spesso frainteso dai medici. Sebbene questo sintomo sia solitamente associato a un infarto miocardico anteriore, può essere causato da altre condizioni non associate a un infarto.
Un piccolo aumento dell'onda R viene rilevato in circa 10% dei pazienti adulti ricoverati ed è la sesta anomalia ECG più comune (19.734 ECG sono stati raccolti dalla Metropolitan Life Insurance Company in un periodo di 5 anni e ¼). Oltretutto, un terzo dei pazienti con un precedente infarto miocardico anteriore può avere solo questo sintomo ECG. Pertanto, la delucidazione degli equivalenti anatomici specifici di questo fenomeno elettrocardiografico è di grande importanza clinica.
Prima di analizzare i cambiamenti nelle onde R, è necessario ricordarne alcuni fondamenti teorici, che sono necessari per comprendere la genesi dell'attivazione ventricolare nelle derivazioni toraciche. La depolarizzazione ventricolare di solito inizia al centro del lato sinistro del setto interventricolare e procede anteriormente e da sinistra a destra. Questo vettore iniziale attività elettrica si manifesta nelle derivazioni toraciche destra e centrale (V1-V3) come una piccola onda r (la cosiddetta " onda settale r").
Piccoli guadagni dell'onda R possono verificarsi quando il vettore di depolarizzazione iniziale diminuisce di grandezza o è diretto all'indietro. Dopo l'attivazione del setto, la depolarizzazione del ventricolo sinistro domina il resto del processo di depolarizzazione. Sebbene la depolarizzazione del ventricolo destro avvenga contemporaneamente a quella sinistra, la sua forza è trascurabile nel cuore di un adulto normale. Il vettore risultante sarà diretto dalle derivazioni V1-V3 e verrà visualizzato come onde S profonde sull'ECG.
Normale distribuzione delle onde R nelle derivazioni toraciche.
Nella derivazione V1, i battiti ventricolari sono di tipo rS, con un aumento costante della dimensione relativa delle onde R rispetto alle derivazioni di sinistra e una diminuzione dell'ampiezza delle onde S. Le derivazioni V5 e V6 tendono a mostrare un qR- tipo complesso, con ampiezza dell'onda R maggiore in V5 che in V6 attenuazione del segnale da parte del tessuto polmonare.Le variazioni normali includono: pattern QS e rSr" stretti in V1 e pattern qRs e R in V5 e V6. Ad un certo punto, di solito in posizione V3 o V4, il complesso QRS inizia a cambiare da prevalentemente negativo a prevalentemente positivo e il R/ Il rapporto S diventa > 1. Questa zona è nota come " zona di transizione ". Alcuni persone sane, la zona di transizione è già visibile in V2. È chiamato " zona di transizione anticipata ". A volte la zona di transizione può essere ritardata fino a V4-V5, questo si chiama " zona di transizione tardiva ", O " ritardo della zona di transizione ".
L'altezza normale dell'onda R nella derivazione V3 è solitamente maggiore di 2 mm
. Se l'altezza delle onde R nelle derivazioni V1-V4 è estremamente piccola, si dice che c'è "un aumento insufficiente o piccolo dell'onda R".
Esistono varie definizioni di piccolo guadagno dell'onda R in letteratura, criteri comeOnde R inferiori a 2-4 mm nelle derivazioni V3 o V4e/o la presenza di regressione dell'onda R (RV4< RV3 или RV3 < RV2 или RV2 < RV1 или любая их комбинация).
Nella necrosi miocardica dovuta a infarto, una certa quantità di tessuto miocardico diventa elettricamente inerte e incapace di generare la normale depolarizzazione. La depolarizzazione dei tessuti ventricolari circostanti in questo momento aumenta (poiché non sono più resistiti) e il vettore di depolarizzazione risultante si riorienta lontano dall'area di necrosi (nella direzione della propagazione senza ostacoli). Con l'infarto miocardico anteriore, le onde Q compaiono nelle derivazioni destra e media (V1-V4). Tuttavia, le onde Q non sono conservate in un numero significativo di pazienti.
In casi documentati di precedente infarto miocardico anteriore, un piccolo aumento dell'onda R viene rilevato nel 20-30% dei casi . Il tempo medio per la completa scomparsa delle onde Q patologiche è di 1,5 anni.
Attira l'attenzione diminuzione dell'ampiezza dell'onda R nella derivazione I . Fino all'85% dei pazienti con un precedente infarto miocardico anteriore e un piccolo aumento dell'onda R hanno entrambi Ampiezza dell'onda R nella derivazione I<= 4 мм , O Ampiezza dell'onda R nella derivazione V3<= 1,5 мм . L'assenza di questi criteri di ampiezza rende improbabile la diagnosi di infarto miocardico anteriore (con l'eccezione del 10%-15% dei casi di infarto miocardico anteriore).
Se c'è un piccolo aumento delle onde R nelle derivazioni toraciche, Ripolarizzazione alterata (cambiamenti dell'onda ST-T) nelle derivazioni V1-V3 aumenterà la probabilità di diagnosticare un vecchio infarto miocardico anteriore.
Altre possibili cause di crescita insufficiente dell'onda R nelle derivazioni toraciche Sono:
- blocco completo / incompleto della gamba sinistra del fascio di His,
- blocco del ramo anteriore della gamba sinistra del fascio di His,
- il fenomeno Wolf-Parkinson-White,
- alcuni tipi di ipertrofia ventricolare destra (specialmente quelli associati alla BPCO),
- ipertrofia ventricolare sinistra
- ipertrofia ventricolare destra tipo C.

|
| MI anteriore acuto |
Un altro motivo comune per un piccolo aumento dell'onda R è la posizione errata degli elettrodi: posizione troppo alta o troppo bassa degli elettrodi del torace, posizione degli elettrodi dagli arti al corpo.
Molto spesso, la posizione elevata degli elettrodi del torace destro porta a una crescita insufficiente delle onde R. Tuttavia, quando gli elettrodi vengono spostati nella posizione normale, viene ripristinata la normale crescita delle onde R nel vecchio infarto miocardico anteriore, i complessi QS persisteranno
.
Sfortunatamente, questi criteri si sono rivelati di scarsa utilità per la diagnosi e danno molti risultati falsi negativi e falsi positivi.
È stata rivelata una connessione tra un piccolo aumento dell'onda R sull'ECG e la disfunzione diastolica nei pazienti con diabete mellito, quindi questo sintomo può essere un segno precoce di disfunzione ventricolare sinistra e DCM nei diabetici.
Riferimenti.
- Elettrocardiografico Scarsa progressione dell'onda R. Correlazione con i risultati dell'autopsia. Michael I. Zema, MD, Margaret Collins, MD; Daniel R. Alonso, MD; Paul Kligfield, M.D.CHEST, 79:2, FEBBRAIO 1981
- Valore diagnostico della scarsa progressione dell'onda R negli elettrocardiogrammi per la cardiomiopatia diabetica nei pazienti diabetici di tipo 2/CARDIOLOGIA CLINICA, 33(9):559-64 (2010)
- Scarsa progressione dell'onda R nelle derivazioni precordiali: implicazioni cliniche per la diagnosi di infarto miocardico NICHOLAS L. DePACE, MD, JAY COLBY, BS, A-HAMID HAKKI, MD, FACC, BRUNOMANNO, MD, LEONARD N. HOROWITZ, MD, FACC , ABDULMASSIH S. ISKANDRIAN, MD, FACC. JACC vol. 2. N. 6 dicembre 1983"1073-9
- Scarsa progressione dell'onda R. J InsurMed 2005;37:58–62. Ross MacKenzie, MD
- Dott. Blog ECG di Smith, lunedì 6 giugno 2011
- Dott. Blog ECG di Smith, martedì 5 luglio 2011
- http://www.learntheheart.com/ ECG con progressione dell'onda R scadente (PRWP).
- http://clinicalparamedic.wordpress.com/ Progressione dell'onda R: è importante? SCOMMETTI!!
Inversione delle onde T negative in pazienti con infarto miocardico acuto come manifestazione di dinamiche ECG false negative.
La sindrome di Kechker si verifica nel 2-5° giorno dell'infarto del miocardio; non è associato a retrombosi e alla comparsa (intensificazione) di segni clinici di insufficienza ventricolare sinistra. In altre parole, non è una ricaduta infarto miocardico. La durata della sindrome di Kechker, di regola, non supera i 3 giorni. Successivamente, l'immagine dell'ECG ritorna all'originale: l'onda T diventa negativa o isoelettrica. Le ragioni di questo pattern ECG sono sconosciute. Sono impressionato dal punto di vista che si tratta di una manifestazione di epistenocardite pericardite; tuttavia, in questa sindrome non si osserva il caratteristico dolore pericardico. La corretta interpretazione della sindrome di Koechker evita interventi medici non necessari come la trombolisi o il PCI. Prevalenza: ~1 caso su 50 di infarto del miocardio.
(sinonimo: fenomeno della memoria) - cambiamenti non specifici nella parte finale del complesso ventricolare (principalmente l'onda T) nelle contrazioni spontanee che compaiono con stimolazione ventricolare destra artificiale (artificiale) prolungata.

La stimolazione artificiale dei ventricoli è accompagnata da una violazione della geometria della loro contrazione. Con una stimolazione più o meno prolungata (da 2-3 mesi), i cambiamenti nel complesso QRS sotto forma di onde T negative in molte derivazioni ECG possono apparire in contrazioni spontanee. Questa dinamica imita i cambiamenti ischemici. D'altra parte, in presenza di dolore veramente anginoso, questo fenomeno rende quasi impossibile diagnosticare un infarto miocardico a focale piccola. Una corretta interpretazione del fenomeno Chaterier consente di evitare inutili ricoveri e interventi medici ingiustificati.
È importante capire che il fenomeno Shaterier può manifestarsi non solo sullo sfondo di una prolungata stimolazione artificiale del cuore: questa è la ragione principale, ma non l'unica. Con blocco di branca cronico, con frequente extrasistole ventricolare o con il fenomeno WPW, anche la parte terminale del complesso ventricolare nelle contrazioni normali può cambiare: si formano onde T negative o di bassa ampiezza.
Pertanto, qualsiasi violazione a lungo termine della geometria della contrazione ventricolare dovuta alla conduzione anomala dell'impulso intraventricolare può essere accompagnata dal fenomeno di Chaterrier.
È stato notato che sull'ECG di persone sane, l'ampiezza dell'onda T in V6 è sempre maggiore dell'ampiezza dell'onda T in V1 di circa 1,5-2 volte. Inoltre, la polarità dell'onda T in V1 non ha importanza. Violazione di questa relazione, quando le ampiezze delle onde T in V1 e V6 "si allineano" o Lattina V1 supera T in V6 è una deviazione dalla norma. Questa sindrome è più spesso osservata nell'ipertensione (a volte è il primo segno di ipertrofia miocardica ventricolare sinistra) e in varie forme cliniche di malattia coronarica. Può anche essere un segno precoce di intossicazione da digitale.



Il significato clinico di questa sindrome: consente di sospettare "non la norma" e, se necessario, continuare la ricerca diagnostica "dal semplice al complesso".
Nella maggior parte dei casi, l'ampiezza dell'onda R nelle derivazioni toraciche "destre" aumenta e per la derivazione V3 raggiunge almeno 3 mm. Nelle situazioni in cui l'ampiezza dell'onda R in V3 è inferiore a 3 mm, è lecito parlare di sindrome di crescita insufficiente dell'onda R da V1 a V3. Questa sindrome può essere suddivisa in 2 categorie:
1. Non ci sono altre anomalie sull'ECG.
Variante norma (più spesso con costituzione iperstenica),
segno di ipertrofia miocardica ventricolare sinistra,
Posizione errata degli elettrodi toracici (V1-V3) sullo spazio intercostale sovrastante.
2. Ci sono altre anomalie sull'ECG.
Tipico per le seguenti situazioni cliniche:
- infarto miocardico nella "mossa" (in questo caso, ci sarà una dinamica ECG caratteristica di un infarto nelle derivazioni V1 -V3),
cardiosclerosi postinfartuale,
Ipertrofia miocardica grave del ventricolo sinistro con altri criteri ECG per l'ipertrofia,
Blocco del LBB (completo o incompleto), blocco del ramo anteriore del LBB,
- Tipo S di ipertrofia ventricolare destra (raro).




La difficoltà nell'interpretazione della sindrome del sottobosco dell'onda R da V1 a V3 si verifica, di norma, se viene diagnosticata come un pattern ECG indipendente e asintomatico e non ci sono altre anomalie sull'ECG. Con gli elettrodi toracici correttamente applicati e l'assenza di storia cardiaca, la sua causa principale è l'ipertrofia miocardica ventricolare moderata.
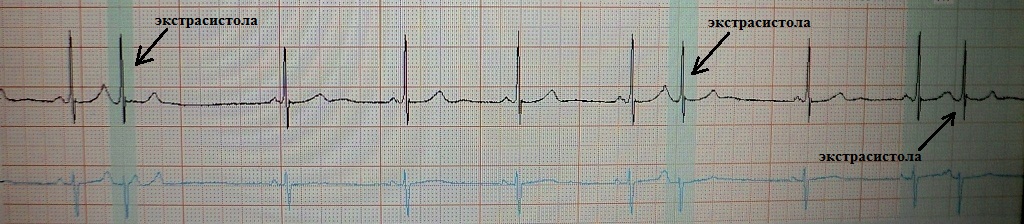
Come sapete, la contrazione prematura del cuore si chiama extrasistole. L'intervallo di accoppiamento di eccitazione extra è più breve ( corto) intervallo tra le contrazioni maggiori. Questo è seguito da una pausa compensativa ( lungo), che è accompagnato da un allungamento della refrattarietà cardiaca e da un aumento della sua dispersione (dispersione della refrattarietà). A questo proposito, immediatamente dopo la contrazione del seno postextrasistolico, esiste la possibilità di un'altra extrasistole ( corto) è il "prodotto" della dispersione della refrattarietà. Il meccanismo dell'extrasistole "ripetuta": rientro o post-depolarizzazione precoce. Esempi:
corto-lungo-corto in un paziente con extrasistole funzionale bradi-dipendente, che in questo caso non ha particolare significato clinico:
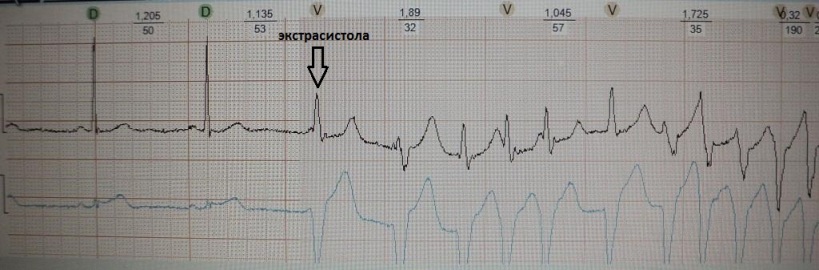
breve-lungo-breve in un paziente con grave sindrome da apnea notturna, obesità e ipertensione 3 cucchiai. Come puoi vedere, dopo una pausa compensatoria, è apparsa un'extrasistole ventricolare polimorfica accoppiata. In questo paziente, il fenomeno breve-lungo-breve può innescare tachicardia ventricolare polimorfa e portare a morte improvvisa:
corto-lungo-corto in un paziente con sindrome del QT lungo: inizio di torsione di punta TV. A volte con questa sindrome, il fenomeno breve-lungo-breve è un prerequisito per l'inizio della tachiaritmia ventricolare:
Nei pazienti con extrasistole funzionale, il fenomeno corto-lungo-corto non ha significato clinico; solo "facilita" l'insorgenza di extrasistole bradidipendente. Nei pazienti con gravi cardiopatie organiche e canalopatie, questo fenomeno può avviare il lancio di aritmie ventricolari pericolose per la vita.
Questo termine si riferisce al periodo del ciclo cardiaco durante il quale la conduzione di un impulso prematuro diventa impossibile (o ritardata), sebbene vengano condotti impulsi con minore prematurità. Le differenze di refrattarietà a diversi livelli del sistema di conduzione del cuore forniscono la base elettrofisiologica per questo fenomeno.
Al primo ECG, vediamo un'extrasistole atriale precoce effettuata ai ventricoli senza aberrazione. Sul secondo ECG, l'intervallo di frizione dell'extrasistole atriale è più lungo, tuttavia l'extrasistole viene eseguita ai ventricoli con un ritardo (aberrazione).
Fondamentalmente, il fenomeno del "gap" viene riscontrato dagli specialisti che eseguono l'EPS del cuore.
- aberrazione a ciclo breve (blocco di fase 3), che si verifica quando il periodo refrattario della giunzione AV aumenta, a causa di un improvviso allungamento dell'intervallo tra due contrazioni precedenti. Più lungo è l'intervallo tra le contrazioni, maggiore è la probabilità di conduzione aberrante (o blocco) del successivo impulso sopraventricolare.
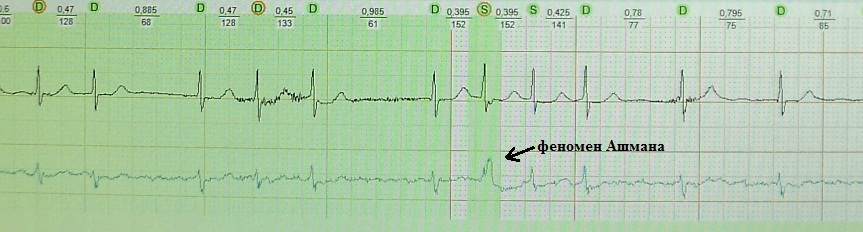
Un classico esempio del fenomeno di Ashman nella fibrillazione atriale:
Il fenomeno di Ashman che si è alzato dopo una pausa compensativa postextrasistolica:
Blocco delle extrasistoli atriali che si sono verificate dopo l'allungamento spontaneo dell'intervallo tra le contrazioni del seno:
Il significato clinico del fenomeno Ashman: la sua corretta interpretazione evita la sovradiagnosi di a) extrasistole ventricolare eb) disturbi della conduzione organica nella giunzione AV.
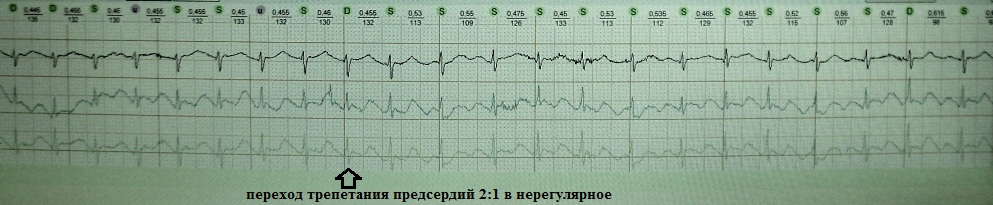
Decorso continuamente ricorrente di fibrillazione atriale parossistica, quando dopo la fine di un attacco, dopo 1-2 contrazioni sinusali, inizia un nuovo parossismo.
caratteristica della fibrillazione atriale vago-dipendente. Da un lato, il fenomeno riflette l'elevata attività ectopica degli accoppiamenti muscolari delle vene polmonari, dall'altro, l'elevata prontezza profibrillatoria del miocardio atriale.
Oltre all'eccitazione retrograda degli atri, esiste la possibilità di penetrazione dell'impulso ventricolare nella connessione AV a una profondità diversa con la sua scarica (prolungamento della refrattarietà, blocco). Di conseguenza, i successivi impulsi sopraventricolari (solitamente da 1 a 3) saranno ritardati (aberrati) o bloccati.
Conduzione VA latente dovuta a PVC, che porta al blocco AV funzionale 1° stadio:
Conduzione VA latente dovuta a PVC, che porta al blocco AV funzionale 2° stadio:
Conduzione VA latente dovuta a PVC, accompagnata da una pausa compensativa posticipata (spostata):

Significato clinico della conduzione VA occulta: la corretta interpretazione di questo fenomeno permette di distinguere tra blocchi AV funzionali e blocchi organici.
Nella maggior parte delle persone, il nodo AV è omogeneo. In alcuni, il nodo AV è elettrofisiologicamente diviso in una zona di conduzione veloce e lenta (dissociata). Se una persona è soggettivamente sana, questo fenomeno non ha significato clinico. Tuttavia, in alcuni pazienti, la dissociazione del nodo AV è accompagnata dallo sviluppo di parossismi di tachicardia AV reciproca nodale. L'innesco della tachicardia è l'extrasistole sopraventricolare, che viene eseguita lungo il percorso veloce e solo retrograda lungo il percorso lento: il circuito di rientro si chiude. Il fenomeno della dissociazione del nodo AV è stabilito in modo affidabile dall'EPS del cuore. Tuttavia, su un ECG di routine, a volte possono essere rilevati segni di una malattia dissociativa.
Si consideri il seguente caso clinico. Una paziente di 30 anni lamenta palpitazioni immotivate. Monitoraggio giornaliero eseguito dell'ECG.
Frammento di un ECG - una variante della norma:
Frammento ECG - Blocco AV 1 cucchiaio. sullo sfondo della tachicardia sinusale - assolutamente non tipico per la norma:
Frammento ECG - Blocco AV 2 cucchiai, Tipo 1. Richiama l'attenzione sul prolungamento "rapido" dell'intervallo PR, seguito dalla perdita dell'onda ventricolare:
Un aumento una tantum dell'intervallo P-R di oltre 80 ms fa pensare alla dissociazione del nodo AV in zone con diverse velocità di conduzione dell'impulso. Questo è ciò che vediamo in questo esempio. Successivamente, il paziente è stato sottoposto a EPS del cuore: è stata verificata tachicardia reciproca AV-nodale. L'ablazione della via lenta del nodo AV è stata eseguita con un buon effetto clinico.
Pertanto, i segni di dissociazione del nodo AV sull'ECG di superficie (alternanza di intervalli P-R normali e prolungati; aumento una tantum dell'intervallo P-R nel periodo Wenckebach di oltre 80 ms) in combinazione con una storia aritmica consentono di stabilire una diagnosi con un'alta probabilità anche prima dell'EPS cardiaco.
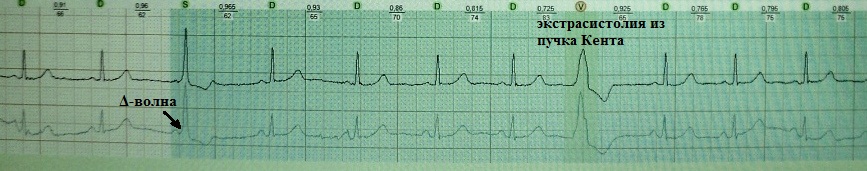
Nonostante tutta l'apparentemente improbabile di questo fenomeno, non è così raro. Il fascio di Kent serve non solo come percorso aggiuntivo per condurre un impulso dagli atri ai ventricoli, ma è anche in grado di possedere automatismo (depolarizzazione diastolica spontanea). L'extrasistole dal fascio di Kent può essere sospettata quando i segni ECG del fenomeno WPW sono combinati con l'ectopia diastolica tardiva, simulando l'extrasistole ventricolare. In questo caso, il complesso ventricolare dilatato è un'onda delta continua.
Si consideri il seguente esempio clinico. Una donna di 42 anni lamentava attacchi di palpitazioni immotivate. Monitoraggio ECG condotto per due giorni. Nel primo giorno dello studio sono stati registrati circa 500 complessi ventricolari "allargati", che compaiono in tarda diastole e scompaiono con un aumento della frequenza cardiaca. A prima vista, un'innocua extrasistole ventricolare funzionale. Tuttavia, l'extrasistole ventricolare diastolica tardiva, essendo dipendente dal calcio, appare principalmente sullo sfondo della tachisistole o immediatamente dopo il suo completamento. In questo caso, i complessi ventricolari tardivi vengono registrati a una frequenza cardiaca normale e con bradicardia, che è già di per sé strana.
La situazione si è completamente chiarita al secondo giorno di monitoraggio, quando si sono manifestati segni di preeccitazione ventricolare intermittente. È diventato chiaro che i complessi ventricolari diastolici tardivi non sono altro che extrasistoli del fascio di Kent.
Il significato clinico dell'extrasistole dal fascio di Kent: la corretta interpretazione di questo fenomeno ci consente di escludere la diagnosi di extrasistole ventricolare e indirizzare il processo diagnostico e terapeutico nella giusta direzione.
Si osserva con tachiaritmie sopraventricolari, specialmente con fibrillazione atriale. L'essenza del fenomeno sta nel fatto che gli impulsi sopraventricolari, arrivando frequentemente e irregolarmente nella giunzione AV, la penetrano a diverse profondità; scaricarlo prima di raggiungere i ventricoli. Di conseguenza, 1) la conduzione dei successivi impulsi sopraventricolari rallenta, 2) l'impulso ectopico sostitutivo rallenta (abbandona).
Sull'ECG di superficie, si può parlare del fenomeno della conduzione AV latente sulla base dei seguenti segni:
Alternanza di intervalli R-R brevi e lunghi nella fibrillazione atriale:
Nessun complesso di scorrimento a intervalli eccessivamente lunghi RR con fibrillazione atriale:
Assenza di complessi di fuga al momento di una pausa di più secondi durante il ripristino del ritmo sinusale:
Quando il flutter atriale regolare si trasforma in fibrillazione atriale irregolare o:
L'extrasistole dalle parti distali della giunzione AV (il tronco del fascio di His) è un tipo di extrasistole ventricolare ed è chiamata "stelo". Designo questo tipo di extrasistole come un fenomeno aritmico, in primo luogo, per la sua relativa rarità, in secondo luogo, per la somiglianza esterna con la tipica extrasistole ventricolare parietale, e in terzo luogo, per la sua refrattarietà ai tradizionali farmaci antiaritmici.
Segni clinici ed elettrocardiografici di extrasistole staminali: 1) il complesso QRS ha più spesso un aspetto sopraventricolare, o è leggermente allargato per aberrazione sporadica o per la vicinanza al tratto prossimale di una delle gambe del fascio di His; 2) l'attivazione atriale retrograda non è tipica; 3) l'intervallo della frizione è variabile, poiché la localizzazione dello stelo del fuoco extrasistolico suggerisce una depolarizzazione calcio-dipendente, cioè un automatismo anormale; 4) assoluta refrattarietà agli antiaritmici di classe I e III.
Esempi:
Con extrasistole staminali, un buon effetto clinico può essere ottenuto solo con l'uso a lungo termine di farmaci antiaritmici di classe II o IV.
- conduzione dell'impulso invece del suo previsto blocco (aberrazione).
Esempio 1:
Probabile meccanismo: l'impulso atriale ha catturato il LBB nella sua fase supernormale.
Esempio #2:
Probabile meccanismo: l'entità del potenziale diastolico spontaneo nel sistema His-Purkinje è massima immediatamente dopo la fine della ripolarizzazione delle contrazioni "seno" (nel nostro caso, sono espanse a causa del blocco del LBB), quindi presto gli impulsi atriali hanno la maggiore possibilità di conduzione "normale".
Esempio n. 3 (fenomeno di Ashman inverso):
Probabile meccanismo: fenomeno di "gap" (fallimento) nella conduzione; accorciamento della refrattarietà con un cambiamento nella lunghezza del ciclo precedente.
Le pause sinusali improvvise sull'ECG non sono sempre facili da interpretare in modo univoco. A volte, per la corretta interpretazione del fenomeno, oltre ad un'approfondita analisi del cardiogramma stesso, è necessaria una valutazione clinica ed anamnestica complessiva. Esempi:
Le pause nell'aritmia sinusale possono essere così pronunciate che c'è un malinteso sulla presenza del blocco SA. Va ricordato che l'aritmia sinusale è asintomatica; è caratteristico principalmente per le persone giovani e di mezza età, comprese le persone soggettivamente sane; appare (si intensifica) con bradicardia (spesso di notte); le pause stesse non sono mai troppo lunghe, provocando così la comparsa di complessi scivolosi; i sintomi cardionevrotici sono un satellite clinico frequente.
Blocco senoatriale di 2° grado:

È necessario scoprire quale tipo di blocco: 1o o 2o. Questa è una domanda fondamentale, poiché la previsione è diversa. Blocco SA 2 cucchiai, il tipo 1 si verifica spesso a riposo (soprattutto di notte) in individui giovani e sani; nei casi classici è preceduto clinicamente ed elettrocardiograficamente dai periodici di Wenkibach; di norma, la pausa non supera il doppio dell'intervallo R-R delle contrazioni precedenti; la presenza di complessi scivolanti non è tipica; nessuna storia sincopale.

Blocco SA di 2° grado, tipo 2 appare improvvisamente senza i periodici di Wenkibach; spesso è presente una concomitante lesione miocardica organica, rilevata strumentalmente; nelle persone anziane, senza evidenti alterazioni cardiache durante l'ECO, la causa principale è la cardiosclerosi; la pausa può essere più lunga del doppio dell'intervallo RR delle contrazioni precedenti; spesso si verificano complessi di scivolamento; è caratteristica una storia di sincope o equivalente.


Extrasistole atriale bloccata:
Di norma, causa difficoltà nella diagnosi solo se il numero di extrasistoli bloccati è piccolo e il numero di quelli ordinari (non bloccati) non supera la norma statistica: questo attenua la vigilanza del medico. La cura elementare nell'analisi dell'ECG verificherà in modo affidabile l'extrasistole atriale bloccata. Nella mia esperienza, un'onda P ectopica bloccata molto presto deforma sempre in una certa misura l'onda T, rendendo possibile la diagnosi di questo fenomeno senza EPS.
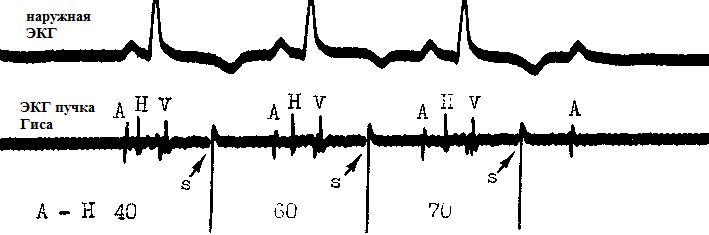
Menzionando l'extrasistole latente in questa sezione, rendo omaggio all'estrema insolitezza di questo fenomeno. Stiamo parlando di extrasistole staminali, che è bloccata antero- e retrograda. Pertanto, non è visibile sull'ECG di superficie. La sua diagnosi è possibile solo con l'elettrocardiografia del fascio di His. Nella figura sopra, la radice extrasistole è provocata artificialmente: stimolo S. Come puoi vedere, gli stimoli S non si propagano oltre la giunzione AV e quindi non sono visibili sull'ECG. Il terzo stimolo imposto provoca un blocco AV transitorio di 2 ° grado ("). Sull'ECG esterno, si può sospettare extrasistole staminali latente se esiste una combinazione di extrasistoli AV convenzionali (cablate) e pause cardiache improvvise del blocco AV di tipo 2 cucchiai .
L'aberrazione con l'aumento della prematurità non sorprende nessuno, poiché è associata a un rapido aumento della frequenza cardiaca, quando la refrattarietà nel sistema di conduzione non ha ancora avuto il tempo di accorciarsi. L'aberrazione appare molto più insolita quando la frequenza cardiaca rallenta, quando sembrerebbe che il periodo refrattario sia ovviamente terminato.

La base per l'aberrazione del ciclo lungo è la capacità delle cellule del sistema di His-Purkinje alla depolarizzazione diastolica spontanea. Pertanto, se c'è una pausa nel lavoro del cuore, il potenziale di membrana in alcune parti del sistema di conduzione del cuore può raggiungere il valore del potenziale di riposo ("ipopolarizzazione critica"), che rallenta o rende impossibile condurre l'impulso successivo. Va inteso che tale situazione riflette quasi sempre una patologia organica del sistema di conduzione, quando le cellule della giunzione AV si trovano già inizialmente in uno stato di ipopolarizzazione (basso valore del massimo potenziale diastolico). Il fenomeno del blocco bradi-dipendente non è caratteristico di un cuore sano e spesso precede disturbi della conduzione più gravi.
Letteralmente significa: la soppressione dei pacemaker con impulsi più frequenti. Questo fenomeno si basa sull'iperpolarizzazione delle cellule automatiche a causa del fatto che vengono attivate più frequentemente della loro stessa frequenza di eccitazione. Possiamo osservare questo fenomeno fisiologico sull'ECG di qualsiasi persona sana, quando il nodo del seno soggioga tutti i pacemaker a valle. Maggiore è la frequenza del ritmo sinusale, minore è la probabilità di comparsa di impulsi eterotopici, inclusa l'extrasistole. D'altra parte, se la frequenza degli impulsi del focus ectopico supera l'automatismo del nodo del seno, allora il nodo del seno stesso subirà la soppressione della superfrequenza. Quest'ultimo fatto attira spesso l'attenzione del medico, poiché la pausa dopo il ripristino del ritmo sinusale può essere eccessivamente lunga. Per esempio:


Quando EFI attraverso il fenomeno della "soppressione dell'overdrive" rivela la disfunzione del nodo del seno.
Inizialmente chiamato extrasistole ventricolare di tipo R su T ed extrasistole atriale di tipo P su T.
Con tutta la probabilità della comparsa di tali extrasistoli in una persona sana (soprattutto atriale), va ricordato che più breve è la prematurità dell'extraeccitazione, meno è tipica del miocardio normale. Pertanto, quando ci si trova di fronte per la prima volta ad una extrasistole precoce, è necessario valutare clinicamente e strumentalmente la presenza di dispersione della refrattarietà miocardica, cioè la probabilità di innesco di tachiaritmie per extrasistole. L'extrasistole atriale precoce, basata sugli accoppiamenti muscolari delle bocche delle vene polmonari, inizia spesso a essere rilevata nelle persone di mezza età. Molto spesso, si manifesta con un meccanismo riflesso come parte di una malattia extracardiaca dovuta a stile di vita sbagliato. E se la causa dell'aritmia non viene eliminata, prima o poi l'extrasistole atriale precoce inizia a scatenare la fibrillazione atriale. La combinazione di battiti prematuri atriali, dilatazione atriale sinistra e ipertensione (o ipertensione arteriosa occulta) è il predittore clinico più affidabile di future tachiaritmie atriali. Nelle persone senili, nella maggior parte dei casi si registra extrasistole atriale precoce.
Una responsabilità molto maggiore ricade sulle spalle del medico nell'analisi clinica dell'extrasistole ventricolare precoce - poiché le aritmie ventricolari potenzialmente letali sono quasi sempre avviate dal fenomeno di R a T. In una persona sana, l'extrasistole ventricolare precoce può essere registrata solo sullo sfondo di un ritmo frequente; con la sua contrazione, diventa mesodiastolico:
Il fenomeno isolato di R su T sullo sfondo della normo- o bradicardia è sempre sospetto in relazione alla sua particolare origine elettrofisiologica: post-depolarizzazione precoce. Come è noto, non ci sono condizioni per post-depolarizzazioni precoci in un miocardio sano (soprattutto nel miocardio ventricolare). Pertanto, se vengono respinte le ovvie cause di extrasistole ventricolare precoce sotto forma di danno miocardico organico acuto o cronico, è necessario escluderne altre - quelle congenite. Permettetemi di ricordarvi che con la cosiddetta cardiopatia elettrica, l'extrasistole ventricolare precoce può essere l'unica manifestazione di patologia latente per lungo tempo.
Non c'è ancora consenso sull'origine dell'onda U. La questione del suo significato clinico rimane discutibile. Ci sono diverse teorie sulla sua origine:
1) L'onda U è causata da potenziali tardivi che seguono i propri potenziali d'azione.
2) L'onda U è causata dai potenziali risultanti dallo stiramento dei muscoli ventricolari durante il periodo di rapido riempimento ventricolare nella prima fase della diastole.
3) L'onda U è causata da potenziali indotti dalla ritardata ripolarizzazione tardiva durante l'allungamento della parete del ventricolo sinistro durante la diastole.
4) L'onda U è dovuta alla ripolarizzazione dei muscoli papillari o delle fibre di Purkinje.
5) L'onda U è causata da oscillazioni elettriche provocate da un'onda meccanica di sufficiente intensità allo sbocco delle vene dopo il passaggio di un normale polso arterioso lungo il circuito chiuso “arteria-vena”.
Pertanto, tutte le teorie si basano sull'esistenza di alcune oscillazioni tardive, che per un breve periodo spostano il potenziale transmembrana del miocardio al momento della diastole precoce verso l'ipopolarizzazione. Mi è più vicina la teoria numero 2. Un miocardio moderatamente ipopolarizzato ha aumentato l'eccitabilità - come sapete, l'onda U sull'ECG coincide cronologicamente con la cosiddetta fase supernormale del ciclo cardiaco, in cui, ad esempio, si verifica facilmente l'extrasistole.
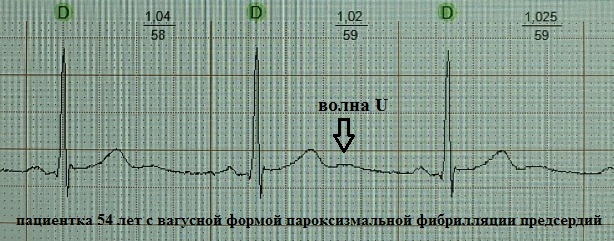
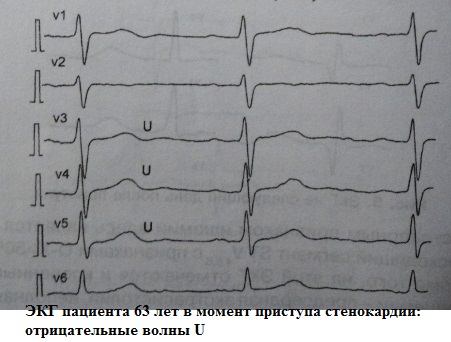
Incerto (e secondo me insignificante) è il significato clinico dell'onda U. Normalmente, l'onda U è un'onda piccola (circa 1,5-2,5 mm sull'ECG), positiva, piatta, che segue l'onda T in 0,02-0,04 secondi ed è meglio visualizzata nelle derivazioni V3, V4. Spesso l'onda U non viene rilevata affatto o "strati" sull'onda T. E, ad esempio, a una frequenza cardiaca superiore a 95-100 battiti al minuto, il suo rilevamento è quasi impossibile a causa della sovrapposizione sull'atriale P Si ritiene che normalmente abbia la massima ampiezza nei giovani adulti sani. Tuttavia, teoricamente può verificarsi in qualsiasi situazione clinica, aumentando di ampiezza con la tachisistole:

Si ritiene che l'onda U negativa non sia assolutamente caratteristica della norma. L'oscillazione U negativa è quasi sempre associata a qualche tipo di patologia. Un'altra cosa è che il valore diagnostico di tale inversione può essere completamente diverso:
È corretto parlare del ruolo di sostituzione ("salvataggio") del ritmo ventricolare solo in quei casi in cui appare sullo sfondo dell'arresto cardiaco nei blocchi SA o AV "parossistici" o nella dissociazione AV passiva. In altre situazioni, abbiamo a che fare con un ritmo idioventricolare accelerato (AVR), che appare come immotivato ("attivamente"). La sua frequenza non supera i 110-120 al minuto, altrimenti viene diagnosticata la tachicardia ventricolare. Ci sono diverse ragioni per l'emergere del SIR:
Sindrome da riperfusione nell'infarto miocardico acuto,
Cardiopatia organica nota con ridotta funzione sistolica del ventricolo sinistro (come parte di un'ectopia più grande potenzialmente maligna),
intossicazione da digitale,
Casi idiopatici in individui sani.
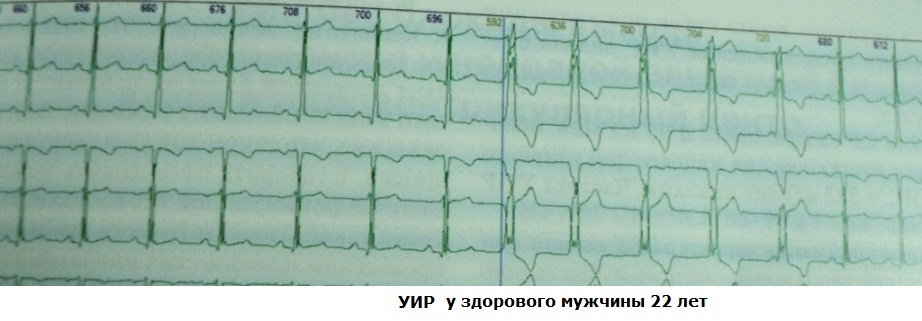
Molto spesso, l'UIR compare nell'infarto miocardico acuto al momento della ricanalizzazione completa o parziale dell'arteria coronaria. In una tale situazione, una grande quantità di calcio entra nei cardiomiociti storditi, che spostano il potenziale transmembrana al livello di soglia (ipopolarizzazione della cellula); di conseguenza, i cardiomiociti acquisiscono la proprietà dell'automazione. È importante sapere che i SIR non sono un criterio affidabile per il successo della riperfusione: la ricanalizzazione può essere parziale o intermittente. Tuttavia, in combinazione con altri segni clinici, il valore prognostico dell'UIR, come marcatore del ripristino del flusso sanguigno coronarico, è piuttosto elevato. I casi di fibrillazione ventricolare "da riperfusione" sono molto rari. Esempi:
La sindrome da riperfusione è affrontata principalmente dai medici della fase ospedaliera che lavorano in cardiorianimazione; i cardiologi policlinici oi medici di diagnostica funzionale hanno maggiori probabilità di occuparsi di altre cause di UIR.
L'intossicazione da digitale, come causa di UIR, è diventata sempre meno comune negli ultimi anni. Ha solo bisogno di essere ricordato.
Di grande importanza clinica è l'identificazione di UIR in pazienti con cardiopatia organica sullo sfondo della disfunzione sistolica del ventricolo sinistro. Qualsiasi ectopia ventricolare in una situazione del genere dovrebbe essere trattata come potenzialmente maligna: aumenta certamente il rischio di morte cardiaca improvvisa attraverso l'inizio della fibrillazione ventricolare, specialmente se si verifica durante il periodo di recupero dopo l'esercizio. Esempio:
Anche 10-15 anni fa, quando registravano l'UIR in persone senza cardiopatie organiche, i cardiologi emettevano un verdetto di prognosi clinica "incerta" - tali soggetti erano sotto il patrocinio medico. Tuttavia, le loro osservazioni a lungo termine hanno dimostrato che l'UIR non aumenta il rischio di morte cardiaca improvvisa e in tali casi è un'aritmia "cosmetica". Spesso, l'UIR in individui sani è associata ad altre anomalie cardiache e non cardiache: il fenomeno WPW, accordi aggiuntivi, sindrome da ripolarizzazione ventricolare precoce, manifestazioni sindrome da displasia del tessuto connettivo. Il significato clinico dell'UIR sarà determinato dalla tolleranza soggettiva dell'aritmia e dal suo effetto sull'emodinamica intracardiaca (la probabilità di sviluppare una dilatazione aritmogena del cuore). Esempi:

Il medico non deve essere confuso da parametri UIR come la variabilità di frequenza e il polimorfismo dei complessi ventricolari. L'irregolarità del ritmo è determinata dall'automatismo interno del centro ectopico o dal blocco dell'uscita con i periodici di Wenckebach. L'apparente politopicità dei complessi ectopici, infatti, non è altro che una conduzione aberrante dell'eccitazione. Secondo l'opinione generale, il meccanismo dell'UIR negli individui sani è un automatismo anormale.
Nella diagnosi differenziale dei ritmi ventricolari accelerati, dovrebbero essere esclusi il fenomeno Ashman, il fenomeno WPW e il blocco di branca dipendente da tachi o bradi.
È una variante del pacemaker ipersensibile ai potenziali dei muscoli scheletrici del torace, del cingolo scapolare, dei muscoli addominali o del diaframma. Di conseguenza, l'elettrodo di rilevamento, percependo i segnali extracardiaci, dà un comando per inibire il prossimo impulso artificiale: si verifica una pausa cardiaca, che può terminare con uno svenimento per il paziente. Di norma, l'inibizione del miopotenziale è provocata da alcune azioni, ad esempio il lavoro attivo con le mani. Questo fenomeno è tipico dei pacemaker con configurazione monopolare dell'elettrocatetere; sono stati impiantati sempre meno negli ultimi anni. Esempi:
Opzioni per correggere l'inibizione del miopotenziale: 1) diminuire la soglia di sensibilità dell'elettrodo, 2) riprogrammare il sistema per una versione di rilevamento bipolare, 3) sostituire l'elettrodo con uno nuovo, con nucleo bipolare.
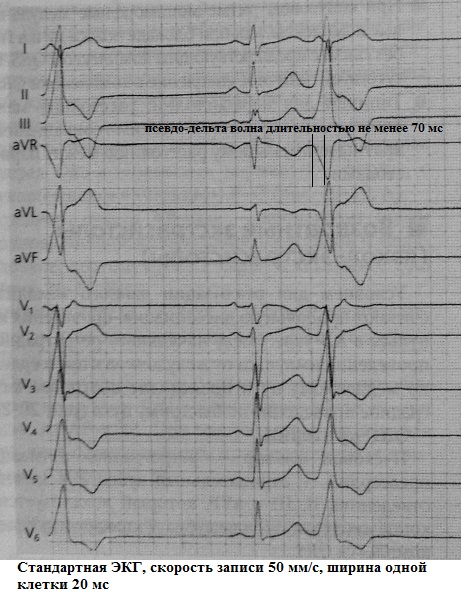
Come è noto, l'onda delta è un segno specifico di preeccitazione ventricolare, dovuto alla presenza di un'ulteriore via di conduzione anterograda senza il ritardo dell'impulso caratteristico del nodo AV. Il solito quadro ECG sotto forma di un'onda delta, che espande il complesso QRS e accorcia l'intervallo P-Q a causa della preeccitazione, è chiamato fenomeno WPW. Tuttavia, a volte c'è una "tentazione" di rilevare un'onda delta dove in realtà non esiste, ma c'è un extrasistole ventricolare, il cui inizio è molto simile alla preeccitazione. Questa è la cosiddetta onda pseudo-delta. Un simile complesso ventricolare imita un'onda delta continua (sinonimi: conduzione antidromica continua, extrasistole dal fascio di Kent). La difficoltà diagnostica si verifica se un'extrasistole ventricolare con un'onda pseudo-delta viene registrata su un ECG standard. Quando si analizza il monitoraggio ECG a lungo termine, tutto va a posto: il fenomeno WPW con extrasistoli dal fascio di Kent (onda delta solida) Sempre sarà combinato con la presenza di complessi ventricolari con una vera onda delta. Al contrario, quando si registra l'extrasistole ventricolare con un'onda pseudo-delta, i segni classici del fenomeno WPW (inclusa la preeccitazione intermittente) non verranno rilevati. Esempi:
Dalla "larghezza" dell'onda pseudo-delta si può giudicare la localizzazione del focus extrasistolico: endocardico o epicardico. L'algoritmo è il seguente: 1) se l'onda pseudo-delta è maggiore di 50 ms, allora possiamo parlare dell'origine epicardica del PVC, 2) se l'onda pseudo-delta è inferiore a 50 ms, allora prestare attenzione al intervallo RS più breve nell'extrasistole su un ECG a 12 derivazioni : la sua durata inferiore a 115 ms indica la localizzazione endocardica del focus, mentre con una durata di 115 ms o più, procedono al terzo passaggio: la presenza di un'onda q in piombo aVL, 3) la presenza di un'onda q in piombo aVL indica l'origine epicardica del PVC, la sua assenza - sull'endocardio. Ad esempio, nell'ECG sottostante, anche secondo i calcoli più approssimativi, la larghezza dell'onda pseudo-delta supera i 50 ms:
La localizzazione del focus extrasistolico interessa non solo gli aritmologi invasivi: con frequenti extrasistoli epicardici, il rischio di sviluppare una dilatazione aritmogena del cuore è molto più alto.
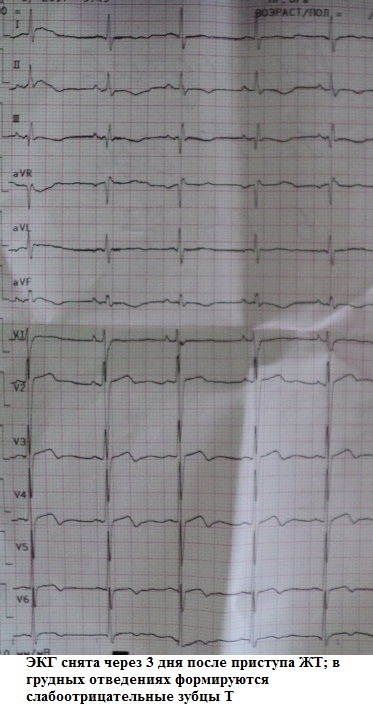
. Con un ritmo cardiaco frequente, vengono mobilitate le risorse energetiche del miocardio. Se un episodio di tachisistole dura troppo a lungo o la frequenza cardiaca è estremamente elevata, il metabolismo intracellulare viene disturbato (non può far fronte al carico) - si forma la distrofia miocardica transitoria. In tal caso, dopo la fine della tachicardia sull'ECG, possono essere rilevati cambiamenti aspecifici nella ripolarizzazione, chiamati sindrome post-tachicardica. Teoricamente, dopo qualsiasi tachicardia (sinusale, sopraventricolare o ventricolare) nel periodo di recupero, possono verificarsi manifestazioni della sindrome post-tachicardica. Nella sua forma classica, è un'inversione transitoria dell'onda T nelle derivazioni precordiali. Tuttavia, l'esperienza pratica mostra che i cambiamenti dell'ECG successivi alla tachicardia possono interessare anche il segmento ST. Pertanto, nella pratica clinica, si verificano le seguenti manifestazioni della sindrome post-tachicardica:
Depressione obliqua-ascendente del segmento S-T con rigonfiamento verso l'alto (come "sovraccarico sistolico"),
- depressione "lenta" obliquo-ascendente del segmento S-T,
Onda T negativa.
La durata della sindrome post-tachicardite è imprevedibilmente variabile: da alcuni minuti a diversi giorni. Con persistente simpaticotonia, le manifestazioni della sindrome post-tachicardica possono esistere per mesi e anni. Un esempio classico è il tipo giovanile di ECG (onde T negative nelle derivazioni V1-V3), caratteristico di adolescenti e giovani con una psiche labile.
Consideriamo brevemente le opzioni per la sindrome post-tachicardite.
La depressione ascendente del segmento S-T con rigonfiamento verso l'alto dopo la tachicardia, di regola, si forma in soggetti con manifestazioni iniziali di ipertrofia miocardica ventricolare sinistra; in tali pazienti, l'ECG a riposo standard ha parametri completamente normali. La depressione più pronunciata si osserva nelle derivazioni V5, V6. Il suo aspetto è familiare a tutti:

Di norma, entro non più di un'ora dall'episodio di tachicardia, l'ECG torna alla normalità. Se l'ipertrofia miocardica progredisce, la normalizzazione del segmento ST viene ritardata per ore o addirittura giorni, e successivamente le manifestazioni di sovraccarico sistolico vengono "fissate" a riposo.
La depressione ascendente obliqua "lenta" del segmento S-T è rara. Molto spesso, appare dopo la tachicardia sullo sfondo di disturbi miocardici funzionali del tipo di NCD.

L'onda T negativa è la variante più comune della sindrome post-tachicardica. È estremamente aspecifico. Faccio tre esempi.
Onde T negative nelle derivazioni precordiali in un ragazzo di 21 anni (può essere considerato un tipo giovanile di ECG) sullo sfondo di persistente simpaticotonia:

Le onde T negative nelle derivazioni toraciche, formate dopo la tachicardia ventricolare:
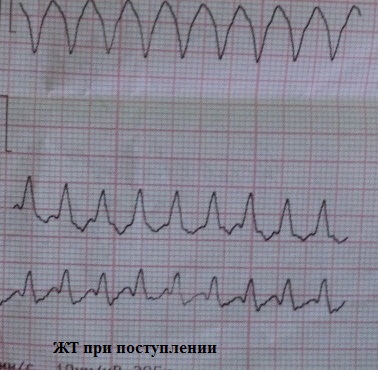
Le onde T negative nelle derivazioni toraciche, formate dopo la tachicardia sopraventricolare:
Significato clinico post-tachicardica la sindrome è fantastica!È una causa frequente di ricoveri e visite mediche inutili. Imitando i cambiamenti ischemici, specialmente in combinazione con sindrome cardiaca, la sindrome posttachicardite può "imitare" la patologia coronarica. Ricordalo! Buona fortuna con la tua diagnosi!
In circa 2/3 delle persone, la gamba sinistra del fascio dei suoi rami non in due rami, ma in tre: anteriore, posteriore e mezzo. Lungo il ramo mediano, l'eccitazione elettrica si estende alla parte anteriore del IVS e parte della parete anteriore del ventricolo sinistro.

Il suo blocco isolato è un evento eccezionalmente raro. Tuttavia, se ciò accade, parte dell'IVS e la parete anteriore del ventricolo sinistro vengono eccitate in modo anomalo, dal lato delle pareti posteriore e laterale del ventricolo sinistro. Di conseguenza, nel piano orizzontale, il vettore elettrico totale sarà diretto in avanti e nelle derivazioni V1-V3 si osserverà la formazione di onde R elevate (complessi qR, R o Rs). Questa condizione deve essere differenziata da:
Sindrome di WPW,
ipertrofia ventricolare destra,
Infarto miocardico posteriore-basale,
ECG normale dei bambini dei primi anni di vita, quando, per motivi naturali, predominano i potenziali del ventricolo destro.
Il blocco del ramo mediano del ramo sinistro del fascio di His può verificarsi sia come parte di un disturbo della conduzione funzionale, sia riflettere indirettamente, ad esempio, una lesione aterosclerotica dell'arteria discendente anteriore, essendo un marker ECG subclinico della malattia coronarica .


L'autore di queste righe ha letteralmente incontrato questo disturbo della conduzione un paio di volte durante la sua attività professionale. Permettetemi di darvi una di queste osservazioni. Il seguente pattern ECG è stato verificato in un paziente sullo sfondo di un forte dolore retrosternale (Fig. A): elevazione obliqua del segmento ST nelle derivazioni aVL, V2 e V3; semiblocco antero-superiore e blocco del ramo mediano della gamba sinistra del fascio di His (onde R di grande ampiezza nelle derivazioni V2, V3). Al di fuori dell'attacco, l'ECG è tornato alla normalità (Fig. B).
All'angiografia coronarica, nel paziente è stato rilevato uno spasmo dell'arteria discendente anteriore nel terzo medio, che è passato con la somministrazione intracoronarica di nitrati; l'aterosclerosi coronarica concentrica era assente. È stata diagnosticata un'angina vasospastica. Pertanto, il blocco del ramo mediano è apparso solo al momento di un attacco anginoso, riflettendo un'ischemia miocardica "profonda".
Come è noto, sindrome da pacemaker può essere provocato da un'interruzione cronicamente esistente della normale sequenza di contrazioni atriali e ventricolari, ad esempio, a causa della conduzione ventricoloatriale o di un ritardo AV inadeguatamente lungo; o la sua manifestazione è associata a non equivalenza emodinamica delle contrazioni cardiache naturali (proprie) e di quelle imposte.
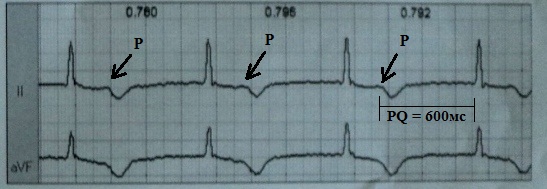
La sindrome da pseudo-pacemaker è un disordine emodinamico dovuto alla presenza di conduzione ventricoloatriale o grave blocco AV di 1° grado con manifestazioni cliniche simili alla sindrome da pacemaker, ma in assenza di stimolazione. Lo sviluppo di questa "pseudo-sindrome" è più spesso osservato con un blocco AV a lungo termine del 1o stadio, superiore a 350-400 ms, quando elettrocardiograficamente l'onda P inizia a sovrapporsi all'intervallo S-T del precedente complesso ventricolare; in questo caso, la sistole atriale si verifica sullo sfondo di una valvola mitrale chiusa.
Permettetemi di darvi un'osservazione letteraria. Il paziente è stato ricoverato in clinica con sintomi di scompenso CHF 4 anni dopo l'impianto del pacemaker in modalità DDDR con una frequenza di stimolazione di base di 50 al minuto. L'ECG ha rivelato il ritmo sinusale con blocco AV 1 cucchiaio. durata circa 600 ms:
La percentuale totale di stimolazione atriale non ha superato il 5%, ventricolare - 7%. In dinamica, è stato riscontrato che rari episodi di ritmo imposto o stimolazione ventricolare P-sincrona sono stati interrotti da extrasistole ventricolare, che è stata nuovamente seguita da ritmo sinusale con grave blocco AV del 1o stadio:
L'algoritmo di funzionamento di questo pacemaker era tale che, dopo ogni contrazione ventricolare, veniva attivato un periodo refrattario atriale di 450 ms e l'onda P appariva circa 200 ms dopo il complesso ventricolare, cioè molto presto e quindi non veniva rilevata. Ciò ha portato alla quasi completa inibizione della stimolazione ventricolare. In questo caso, era necessario accorciare il periodo refrattario atriale o provocare lo sviluppo di un blocco AV completo. A questo paziente, oltre alla terapia di base per l'insufficienza cardiaca, sono state prescritte alte dosi di Verapamil, che, bloccando la conduzione AV, hanno portato al fatto che le contrazioni ventricolari sono diventate imposte al 100% (stimolazione P-sincrona). Il blocco AV medico si è rivelato un fattore decisivo: ha permesso di eliminare la desincronizzazione nella contrazione degli atri e dei ventricoli, dopodiché i fenomeni di insufficienza cardiaca sono stati interrotti.
In questo esempio, vediamo come un blocco AV pronunciato a lungo termine di 1 cucchiaio. può portare allo sviluppo di insufficienza cardiaca.
A volte con la sindrome pseudo-pacemaker, è possibile osservare il fenomeno del "salto" dell'onda P ( P-saltato) quando, sullo sfondo di un pronunciato rallentamento della conduzione AV, l'onda P non si limita a “dissolversi” nel complesso QRS, ma lo precede.
- variazione della lunghezza dell'intervallo RR sotto l'influenza della contrazione ventricolare in assenza di conduzione ventricoloatriale. Si ritiene tradizionalmente che questa aritmia si verifichi quando il numero di onde P sinusali supera il numero di complessi QRS ventricolari, ovvero con blocco AV di 2o o 3o grado. Allo stesso tempo, l'intervallo PP, che include il complesso QRS, diventa più breve dell'intervallo PP libero da contrazione ventricolare:

Tuttavia, l'aritmia ventricolofase sinusale può essere osservata con extrasistole ventricolare, stimolazione ventricolare artificiale. Per esempio:
Il meccanismo più probabile per questo fenomeno è lo stiramento atriale durante la sistole ventricolare, che causa stimolazione meccanica del nodo senoauricolare.
Negli ultimi anni l'approccio clinico ed elettrocardiografico alla sindrome da ripolarizzazione ventricolare precoce ha subito notevoli cambiamenti. Secondo l'opinione consensuale degli esperti, in assenza di manifestazioni cliniche (parossismi di tachicardia ventricolare polimorfica o fibrillazione ventricolare), questa sindrome è correttamente chiamata modello di ripolarizzazione ventricolare precoce, sottolineando così la sua attuale bontà nel quadro di un'innocua anomalia dell'ECG. Termine sindrome Si consiglia di utilizzare RRG soltanto nei pazienti sintomatici affetti da sincope o affetti da morte cardiaca improvvisa attraverso il meccanismo della tachiaritmia ventricolare. Data l'eccezionale rarità di questo corso del fenomeno GERD (~ 1 per 10.000 persone), l'uso del termine modello dovrebbe essere considerata non solo una priorità, ma l'unica corretta.
I criteri per la diagnosi del modello RGC sono diventati più rigorosi. È errato presumere che l'elevazione concava del segmento S-T sia uno dei marcatori di GC.Soggetto ad analisi solo deformazione della parte discendente dell'onda R: la presenza di una tacca (onda j) su di esso o la sua levigatezza si riferisce al modello RRJ. La distanza dall'isoline (il punto di riferimento è la posizione dell'intervallo P-Q) alla sommità della tacca o all'inizio della levigatezza deve essere di almeno 1 mm in due o più derivazioni ECG standard consecutive (escluse le derivazioni aVR, V1-V3 ); la larghezza del complesso QRS deve essere inferiore a 120 ms e il calcolo della durata del QRS viene eseguito solo nelle derivazioni in cui il pattern RGC è assente.


Secondo i criteri sopra descritti, solo l'ECG n. 1 ha un pattern PGC:
Sfortunatamente, non ci sono ancora criteri affidabili per la potenziale malignità del modello RGC e la possibilità della sua transizione alla sindrome. Tuttavia, in presenza dei seguenti segni clinici, un soggetto con un pattern di PPJ dovrebbe essere sotto controllo medico:
Variazione dinamica dell'elevazione del punto j in assenza di variazione della frequenza cardiaca,
La presenza di extrasistoli ventricolari del tipo "da R a T",
La presenza di sincope, presumibilmente diversa nel decorso clinico da vasovagale (cioè svenimento come "all'improvviso ero sul pavimento"),
Morte inspiegabile in un parente di primo grado di età inferiore a 45 anni con quadro documentato di GC
Presenza di pattern RRJ nella maggior parte delle derivazioni (aVR, V1-V3 - non considerato),
Transizione dell'onda j in un segmento orizzontale o discendente S-T.
Per determinare la natura del segmento S-T (ascendente, orizzontale o discendente), si confrontano la posizione del punto Jt e il punto sul segmento S-T, a 100 ms di distanza da esso:
Il rilevamento del blocco AV di 2 ° grado di tipo Mobits II è quasi sempre un segno prognostico sfavorevole, poiché la sua presenza, in primo luogo, riflette un disturbo della conduzione distale al nodo AV e, in secondo luogo, funge spesso da presagio dello sviluppo di una più grave insufficienza dromotropica , ad esempio, blocco AV completo.
Allo stesso tempo, nella cardiologia pratica, c'è una significativa sovradiagnosi del blocco AV del 2o stadio. Mobitz II tipo. Considera le situazioni che possono imitare un tale blocco - il cosiddetto pseudo-Mobitz II (falso blocco AV di II grado di tipo II):
Periodici nodali AV lunghi nel blocco AV di II grado di tipo I;

Improvviso aumento transitorio del tono del nervo vago;

Nascosto ;
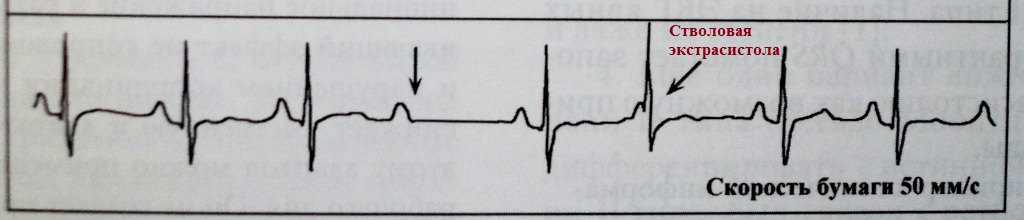
Dopo extrasistole ventricolare;

Sindrome WPW;

Differenza potenziale tra aree adiacenti del sincizio miocardico nella fase di ripolarizzazione del ciclo cardiaco. In un miocardio sano la dispersione della refrattarietà è minima e il suo significato clinico tende a zero. Parlando della presenza di dispersione della refrattarietà miocardica in un paziente, noi a priori implicano un alto rischio di sviluppare aritmia profibrillatoria.
Lo sviluppo di una dispersione clinicamente significativa della refrattarietà è possibile in 2 casi: 1) la presenza di una cardiopatia organica con grave disfunzione sistolica; 2) violazioni del trasporto ionico (canalopatia, squilibrio elettrolitico). In entrambi i casi, la distribuzione dell'eccitazione elettrica in tutte le fasi del ciclo cardiaco non sarà omogenea, il che significa che al momento della ripolarizzazione (refrattarietà relativa), sorgono le condizioni per l'emergere di un potenziale d'azione prematuro - che è elettrocardiograficamente equivalente a una contrazione extrasistolica. Il fronte di eccitazione extrasistolico sarà altrettanto asincrono, quindi, durante la ripolarizzazione, vi è un'alta probabilità di comparsa di un'altra extrasistole, ecc., Fino al decadimento della successiva onda elettrica in più onde e allo sviluppo dell'attività fibrillatoria nel atri o ventricoli.
Esempio 1. Nell'infarto miocardico acuto, un'altra TV polimorfica innescata da PVC, che si è trasformata in FV:
Esempio 2. Paziente con grave ipokaliemia (1,7 mmol/l). Intervallo QT "gigante" (~ 750 ms). In questo contesto compaiono frequenti contrazioni ectopiche politopiche. Alto rischio di sviluppare fibrillazione ventricolare:

La dispersione della refrattarietà, sebbene sia un concetto elettrofisiologico, è più spesso utilizzata dai clinici in senso descrittivo come marker di un aumentato rischio di tachiaritmie ventricolari potenzialmente letali, verificate sulla base della presenza di segni strumentali di disfunzione sistolica ventricolare sinistra. Ad eccezione di alcuni disturbi del trasporto ionico, la dispersione della refrattarietà non ha manifestazioni ECG dirette.
7.2.1. Ipertrofia miocardica
La causa dell'ipertrofia, di regola, è un carico eccessivo sul cuore, sia per resistenza (ipertensione arteriosa) che per volume (renale cronico e / o insufficienza cardiaca). L'aumento del lavoro del cuore porta ad un aumento dei processi metabolici nel miocardio ed è successivamente accompagnato da un aumento del numero di fibre muscolari. L'attività bioelettrica della parte ipertrofica del cuore aumenta, che si riflette nell'elettrocardiogramma.
7.2.1.1. Ipertrofia atriale sinistra
Un segno caratteristico dell'ipertrofia atriale sinistra è un aumento della larghezza dell'onda P (più di 0,12 s). Il secondo segno è un cambiamento nella forma dell'onda P (due gobbe con predominanza del secondo picco) (Fig. 6).
Riso. 6. ECG con ipertrofia atriale sinistra
L'ipertrofia atriale sinistra è un sintomo tipico della stenosi della valvola mitrale e pertanto l'onda P in questa malattia è chiamata P-mitrale. Cambiamenti simili si osservano nelle derivazioni I, II, aVL, V5, V6.
7.2.1.2. Ipertrofia atriale destra
Con l'ipertrofia dell'atrio destro, i cambiamenti interessano anche l'onda P, che acquista una forma appuntita e aumenta di ampiezza (Fig. 7).
Riso. 7. ECG con ipertrofia dell'atrio destro (P-pulmonale), ventricolo destro (tipo S)
L'ipertrofia dell'atrio destro è osservata con difetto del setto interatriale, ipertensione della circolazione polmonare.
Molto spesso, tale onda P viene rilevata nelle malattie dei polmoni, viene spesso chiamata P-pulmonale.
L'ipertrofia dell'atrio destro è un segno di un cambiamento nell'onda P nelle derivazioni II, III, aVF, V1, V2.
7.2.1.3. Ipertrofia ventricolare sinistra
I ventricoli del cuore si adattano meglio ai carichi e nelle prime fasi della loro ipertrofia potrebbero non apparire sull'ECG, ma con lo sviluppo della patologia diventano visibili i segni caratteristici.
Con l'ipertrofia ventricolare, ci sono significativamente più cambiamenti sull'ECG che con l'ipertrofia atriale.
I principali segni di ipertrofia ventricolare sinistra sono (Fig. 8):
Deviazione dell'asse elettrico del cuore a sinistra (levogramma);
Spostamento della zona di transizione verso destra (nelle derivazioni V2 o V3);
L'onda R nelle derivazioni V5, V6 è alta e di ampiezza maggiore rispetto a RV4;
S profondo nelle derivazioni V1, V2;
Complesso QRS esteso nelle derivazioni V5, V6 (fino a 0,1 s o più);
Spostamento del segmento S-T al di sotto della linea isoelettrica con un rigonfiamento verso l'alto;
Onda T negativa nelle derivazioni I, II, aVL, V5, V6.
Riso. 8. ECG con ipertrofia ventricolare sinistra
L'ipertrofia ventricolare sinistra è spesso osservata nell'ipertensione arteriosa, nell'acromegalia, nel feocromocitoma, così come nell'insufficienza delle valvole mitrale e aortica, difetti cardiaci congeniti.
7.2.1.4. Ipertrofia ventricolare destra
Segni di ipertrofia ventricolare destra compaiono sull'ECG nei casi avanzati. La diagnosi in una fase iniziale dell'ipertrofia è estremamente difficile.
Segni di ipertrofia (Fig. 9):
Deviazione dell'asse elettrico del cuore a destra (rightogram);
Onda S profonda nella derivazione V1 e onda R alta nelle derivazioni III, aVF, V1, V2;
L'altezza del dente RV6 è inferiore al normale;
Complesso QRS esteso nelle derivazioni V1, V2 (fino a 0,1 s o più);
Onda S profonda in vantaggio V5 e V6;
spostamento del segmento S-T al di sotto dell'isolina con un rigonfiamento verso l'alto nel III, aVF, V1 e V2 di destra;
Blocco completo o incompleto della gamba destra del fascio di His;
Spostamento della zona di transizione a sinistra.
Riso. 9. ECG con ipertrofia ventricolare destra
L'ipertrofia ventricolare destra è più spesso associata ad un aumento della pressione nella circolazione polmonare nelle malattie polmonari, stenosi della valvola mitrale, trombosi parietale e stenosi dell'arteria polmonare e difetti cardiaci congeniti.
7.2.2. Disturbi del ritmo
Debolezza, mancanza di respiro, palpitazioni, respirazione rapida e difficile, battito cardiaco irregolare, sensazione di soffocamento, svenimento o episodi di perdita di coscienza possono essere manifestazioni di disturbi del ritmo cardiaco dovuti a malattie cardiovascolari. Un ECG aiuta a confermare la loro presenza e, soprattutto, a determinarne il tipo.
Va ricordato che l'automatismo è una proprietà unica delle cellule del sistema di conduzione del cuore, e il nodo del seno, che controlla il ritmo, ha il massimo automatismo.
I disturbi del ritmo (aritmie) vengono diagnosticati quando non c'è ritmo sinusale sull'ECG.
Segni di ritmo sinusale normale:
La frequenza delle onde P è compresa tra 60 e 90 (in 1 min);
La stessa durata degli intervalli RR;
Onda P positiva in tutte le derivazioni tranne aVR.
I disturbi del ritmo cardiaco sono molto diversi. Tutte le aritmie sono suddivise in nomotopiche (i cambiamenti si sviluppano nel nodo del seno stesso) ed eterotopiche. In quest'ultimo caso, gli impulsi eccitatori si verificano al di fuori del nodo del seno, cioè negli atri, nella giunzione atrioventricolare e nei ventricoli (nei rami del fascio di His).
Le aritmie nomotopiche includono bradicardia e tachicardia sinusali e ritmo sinusale irregolare. A eterotopico - fibrillazione atriale e flutter e altri disturbi. Se l'insorgenza di aritmia è associata a una violazione della funzione di eccitabilità, tali disturbi del ritmo sono suddivisi in extrasistole e tachicardia parossistica.
Considerando tutta la varietà di tipi di aritmie che possono essere rilevate sull'ECG, l'autore, per non annoiare il lettore con le complessità della scienza medica, si è permesso solo di definire i concetti di base e considerare i disturbi del ritmo e della conduzione più significativi .
7.2.2.1. Tachicardia sinusale
Aumento della generazione di impulsi nel nodo del seno (più di 100 impulsi per 1 min).
Sull'ECG si manifesta con la presenza di un'onda P regolare e un accorciamento dell'intervallo R-R.
7.2.2.2. Bradicardia sinusale
La frequenza di generazione degli impulsi nel nodo del seno non supera i 60.
Sull'ECG si manifesta con la presenza di un'onda P regolare e un allungamento dell'intervallo R-R.
Va notato che a un tasso inferiore a 30 la bradicardia non è sinusale.
Come nel caso della tachicardia e della bradicardia, il paziente viene trattato per la malattia che ha causato il disturbo del ritmo.
7.2.2.3. Ritmo sinusale irregolare
Gli impulsi sono generati irregolarmente nel nodo del seno. L'ECG mostra onde e intervalli normali, ma la durata degli intervalli R-R differisce di almeno 0,1 s.
Questo tipo di aritmia può verificarsi in persone sane e non necessita di trattamento.
7.2.2.4. Ritmo idioventricolare
Aritmia eterotopica, in cui il pacemaker è costituito dalle gambe del fascio di fibre di His o di Purkinje.
Patologia estremamente grave.
Un ritmo raro sull'ECG (ovvero 30-40 battiti al minuto), l'onda P è assente, i complessi QRS sono deformati ed espansi (durata 0,12 s o più).
Si verifica solo nelle malattie cardiache gravi. Un paziente con tale disturbo necessita di cure urgenti ed è soggetto a ricovero immediato in terapia intensiva cardiologica.
7.2.2.5. Extrasistole
Straordinaria contrazione del cuore causata da un singolo impulso ectopico. Di importanza pratica è la divisione delle extrasistoli in sopraventricolare e ventricolare.
L'extrasistole sopraventricolare (chiamata anche atriale) viene registrata sull'ECG se il fuoco che provoca un'eccitazione straordinaria (contrazione) del cuore si trova negli atri.
L'extrasistole ventricolare viene registrata sul cardiogramma durante la formazione di un fuoco ectopico in uno dei ventricoli.
L'extrasistole può essere raro, frequente (più del 10% delle contrazioni cardiache in 1 minuto), accoppiato (bigemenia) e di gruppo (più di tre di seguito).
Elenchiamo i segni ECG di extrasistole atriale:
Modificato nella forma e nell'ampiezza dell'onda P;
Intervallo P-Q accorciato;
Il complesso QRS registrato prematuramente non differisce nella forma dal complesso normale (seno);
L'intervallo RR che segue l'extrasistole è più lungo del solito, ma più breve di due intervalli normali (pausa compensatoria incompleta).
Le extrasistoli atriali sono più comuni nelle persone anziane sullo sfondo della cardiosclerosi e della malattia coronarica, ma possono anche essere osservate in persone praticamente sane, ad esempio, se una persona è molto preoccupata o stressata.
Se si osserva un extrasistole in una persona praticamente sana, il trattamento consiste nel prescrivere valocordin, corvalol e garantire un riposo completo.
Quando si registra un extrasistole in un paziente, sono richiesti anche il trattamento della malattia di base e l'assunzione di farmaci antiaritmici dal gruppo isoptina.
Segni di extrasistole ventricolare:
L'onda P è assente;
Lo straordinario complesso QRS è notevolmente espanso (più di 0,12 s) e deformato;
Pausa compensatoria completa.
L'extrasistole ventricolare indica sempre danni al cuore (CHD, miocardite, endocardite, infarto, aterosclerosi).
Con extrasistole ventricolare con una frequenza di 3-5 contrazioni per 1 minuto, la terapia antiaritmica è obbligatoria.
Molto spesso viene somministrata la lidocaina per via endovenosa, ma possono essere utilizzati anche altri farmaci. Il trattamento viene effettuato con un attento monitoraggio dell'ECG.
7.2.2.6. Tachicardia parossistica
Attacco improvviso di contrazioni iperfrequenti che durano da pochi secondi a diversi giorni. Il pacemaker eterotopico si trova nei ventricoli o sopraventricolare.
Con la tachicardia sopraventricolare (in questo caso si formano impulsi negli atri o nel nodo atrioventricolare), il ritmo corretto viene registrato sull'ECG con una frequenza da 180 a 220 contrazioni per 1 minuto.
I complessi QRS non vengono modificati o espansi.
Con la forma ventricolare della tachicardia parossistica, le onde P possono cambiare il loro posto sull'ECG, i complessi QRS sono deformati ed espansi.
La tachicardia sopraventricolare si verifica nella sindrome di Wolff-Parkinson-White, meno spesso nell'infarto miocardico acuto.
La forma ventricolare della tachicardia parossistica viene rilevata in pazienti con infarto del miocardio, con malattia coronarica e disturbi elettrolitici.
7.2.2.7. Fibrillazione atriale (fibrillazione atriale)
Una varietà di aritmie sopraventricolari causate da un'attività elettrica asincrona e scoordinata degli atri, seguita da un deterioramento della loro funzione contrattile. Il flusso degli impulsi non è condotto ai ventricoli nel loro insieme, che si contraggono irregolarmente.
Questa aritmia è una delle aritmie cardiache più comuni.
Si verifica in più del 6% dei pazienti di età superiore ai 60 anni e nell'1% dei pazienti di età inferiore a questa età.
Segni di fibrillazione atriale:
gli intervalli R-R sono diversi (aritmia);
Le onde P sono assenti;
Vengono registrate le onde di sfarfallio F (sono particolarmente chiaramente visibili nelle derivazioni II, III, V1, V2);
Alternanza elettrica (diversa ampiezza delle onde I in una derivazione).
La fibrillazione atriale si verifica con stenosi mitralica, tireotossicosi e cardiosclerosi e spesso con infarto del miocardio. L'assistenza medica consiste nel ripristinare il ritmo sinusale. Vengono utilizzati novocainamide, preparati di potassio e altri farmaci antiaritmici.
7.2.2.8. flutter atriale
È osservato molto meno frequentemente della fibrillazione atriale.
Con flutter atriale, l'eccitazione e la contrazione atriali normali sono assenti e si osservano eccitazione e contrazione delle singole fibre atriali.
7.2.2.9. fibrillazione ventricolare
La violazione più pericolosa e grave del ritmo, che porta rapidamente all'arresto circolatorio. Si verifica con infarto del miocardio, così come nelle fasi terminali di varie malattie cardiovascolari in pazienti che si trovano in uno stato di morte clinica. La fibrillazione ventricolare richiede la rianimazione immediata.
Segni di fibrillazione ventricolare:
Assenza di tutti i denti del complesso ventricolare;
Registrazione delle onde di fibrillazione in tutte le derivazioni con una frequenza di 450-600 onde per 1 min.
7.2.3. Disturbi della conduzione
I cambiamenti nel cardiogramma che si verificano in caso di violazione della conduzione di un impulso sotto forma di rallentamento o completa cessazione della trasmissione dell'eccitazione sono chiamati blocchi. I blocchi sono classificati in base al livello in cui si è verificata la violazione.
Assegni blocco sinusovy, predserdny, predserdny e intraventricular. Ciascuno di questi gruppi è ulteriormente suddiviso. Quindi, ad esempio, ci sono blocchi senoatriali di I, II e III grado, blocchi delle gambe destra e sinistra del suo fascio. C'è anche una divisione più dettagliata (blocco del ramo anteriore della gamba sinistra del fascio di His, blocco incompleto della gamba destra del fascio di His). Tra i disturbi della conduzione registrati dall'ECG, i seguenti blocchi sono della massima importanza pratica:
Grado senoatriale III;
Atrioventricolare I, II e III grado;
Blocco delle gambe destra e sinistra del fascio di His.
7.2.3.1. Blocco senoatriale di III grado
Disturbo della conduzione, in cui la conduzione dell'eccitazione dal nodo del seno agli atri è bloccata. Su un ECG apparentemente normale, un'altra contrazione si interrompe improvvisamente (blocchi), cioè l'intero complesso P-QRS-T (o 2-3 complessi contemporaneamente). Al loro posto viene registrata un'isolina. La patologia è osservata in coloro che soffrono di malattia coronarica, infarto, cardiosclerosi, con l'uso di numerosi farmaci (ad esempio beta-bloccanti). Il trattamento consiste nel trattamento della malattia di base e nell'uso di atropina, izadrin e agenti simili).
7.2.3.2. Blocco atrioventricolare
Violazione della conduzione dell'eccitazione dal nodo del seno attraverso la connessione atrioventricolare.
Il rallentamento della conduzione atrioventricolare è un blocco atrioventricolare di primo grado. Appare sull'ECG sotto forma di un prolungamento dell'intervallo P-Q (più di 0,2 s) con una frequenza cardiaca normale.
Blocco atrioventricolare di II grado - blocco incompleto, in cui non tutti gli impulsi provenienti dal nodo del seno raggiungono il miocardio ventricolare.
Sull'ECG si distinguono i seguenti due tipi di blocco: il primo è Mobitz-1 (Samoilov-Wenckebach) e il secondo è Mobitz-2.
Segni di blocco tipo Mobitz-1:
Intervallo in costante allungamento P
A causa del primo segno, a un certo punto dopo l'onda P, il complesso QRS scompare.
Un segno di blocco del tipo Mobitz-2 è un prolasso periodico del complesso QRS sullo sfondo di un intervallo P-Q esteso.
Blocco atrioventricolare di III grado - una condizione in cui non viene condotto ai ventricoli un singolo impulso proveniente dal nodo del seno. Sull'ECG vengono registrati due tipi di ritmo che non sono interconnessi; il lavoro dei ventricoli (complessi QRS) e degli atri (onde P) non è coordinato.
Il blocco dell'III grado si trova spesso nella cardiosclerosi, nell'infarto del miocardio, nell'uso improprio dei glicosidi cardiaci. La presenza di questo tipo di blocco in un paziente è un'indicazione per il suo ricovero urgente in un ospedale cardiologico. Il trattamento prevede atropina, efedrina e, in alcuni casi, prednisolone.
7.2.3.3. Blocco delle gambe del fascio di His
In una persona sana, un impulso elettrico originato dal nodo del seno, passando attraverso le gambe del fascio di His, eccita contemporaneamente entrambi i ventricoli.
Con il blocco della gamba destra o sinistra del fascio di His, il percorso dell'impulso cambia e quindi l'eccitazione del ventricolo corrispondente viene ritardata.
È anche possibile il verificarsi di blocchi incompleti e dei cosiddetti blocchi dei rami anteriore e posteriore del fascio del suo fascio.
Segni di un blocco completo della gamba destra del fascio di His (Fig. 10):
Complesso QRS deformato ed esteso (più di 0,12 s);
Onda T negativa nelle derivazioni V1 e V2;
Segmento S-T sfalsato rispetto all'isolinea;
Allargamento e divisione del QRS nelle derivazioni V1 e V2 come RsR.
Riso. 10. ECG con blocco completo della gamba destra del fascio di His
Segni di un blocco completo della gamba sinistra del fascio di His:
Il complesso QRS è deformato ed espanso (più di 0,12 s);
Offset del segmento S-T dall'isolinea;
Onda T negativa nelle derivazioni V5 e V6;
Espansione e spaccatura del complesso QRS nelle derivazioni V5 e V6 sotto forma di RR;
Deformazione ed espansione del QRS nelle derivazioni V1 e V2 sotto forma di rS.
Questi tipi di blocchi si riscontrano nelle lesioni cardiache, nell'infarto miocardico acuto, nella cardiosclerosi aterosclerotica e miocardica, con l'uso scorretto di una serie di farmaci (glicosidi cardiaci, novocainamide).
I pazienti con blocco intraventricolare non necessitano di terapia speciale. Vengono ricoverati per curare la malattia che ha causato il blocco.
7.2.4. Sindrome di Wolff-Parkinson-White
Per la prima volta una tale sindrome (WPW) fu descritta dagli autori sopra citati nel 1930 come una forma di tachicardia sopraventricolare, che si osserva nei giovani sani ("blocco funzionale del fascio del suo fascio").
È stato ormai stabilito che a volte nel corpo, oltre al normale percorso di conduzione dell'impulso dal nodo del seno ai ventricoli, sono presenti fasci aggiuntivi (Kent, James e Maheim). Attraverso questi percorsi, l'eccitazione raggiunge più velocemente i ventricoli del cuore.
Esistono diversi tipi di sindrome di WPW. Se l'eccitazione entra prima nel ventricolo sinistro, sull'ECG viene registrata la sindrome WPW di tipo A. Nel tipo B, l'eccitazione entra prima nel ventricolo destro.
Segni della sindrome di WPW di tipo A:
L'onda delta sul complesso QRS è positiva nelle derivazioni del torace destro e negativa in quella sinistra (risultato dell'eccitazione prematura di una parte del ventricolo);
La direzione dei denti principali nelle derivazioni del torace è approssimativamente la stessa del blocco della gamba sinistra del fascio di His.
Segni della sindrome di WPW di tipo B:
Intervallo P-Q accorciato (meno di 0,11 s);
Il complesso QRS è espanso (più di 0,12 s) e deformato;
L'onda delta negativa per il torace destro conduce, positiva per il sinistro;
La direzione dei denti principali nelle derivazioni del torace è approssimativamente la stessa del blocco della gamba destra del fascio di His.
È possibile registrare un intervallo P-Q bruscamente accorciato con un complesso QRS non deformato e l'assenza di un'onda delta (sindrome di Laun-Ganong-Levin).
I pacchetti aggiuntivi vengono ereditati. In circa il 30-60% dei casi non si manifestano. Alcune persone possono sviluppare parossismi di tachiaritmie. In caso di aritmia, l'assistenza medica è fornita secondo le regole generali.
7.2.5. Ripolarizzazione ventricolare precoce
Questo fenomeno si verifica nel 20% dei pazienti con patologia cardiovascolare (il più delle volte si verifica nei pazienti con aritmie sopraventricolari).
Non è una malattia, ma i pazienti con malattie cardiovascolari che hanno questa sindrome hanno da 2 a 4 volte più probabilità di soffrire di disturbi del ritmo e della conduzione.
I segni della ripolarizzazione ventricolare precoce (Fig. 11) includono:
elevazione del segmento ST;
Onda delta tardiva (tacca sulla parte discendente dell'onda R);
Denti ad alta ampiezza;
Onda P a doppia gobba di durata e ampiezza normali;
Accorciamento degli intervalli PR e QT;
Aumento rapido e acuto dell'ampiezza dell'onda R nelle derivazioni del torace.
Riso. 11. ECG nella sindrome da ripolarizzazione ventricolare precoce
7.2.6. Ischemia cardiaca
Nella malattia coronarica (CHD), l'afflusso di sangue al miocardio è compromesso. Nelle prime fasi, potrebbero non esserci cambiamenti sull'elettrocardiogramma, nelle fasi successive sono molto evidenti.
Con lo sviluppo della distrofia miocardica, l'onda T cambia e compaiono segni di cambiamenti diffusi nel miocardio.
Questi includono:
Ridurre l'ampiezza dell'onda R;
depressione del segmento S-T;
Onda T bifasica, moderatamente dilatata e piatta in quasi tutte le derivazioni.
L'IHD si verifica in pazienti con miocardite di varia origine, nonché alterazioni distrofiche nel miocardio e cardiosclerosi aterosclerotica.
7.2.7. angina pectoris
Con lo sviluppo di un attacco di angina all'ECG, è possibile rilevare uno spostamento nel segmento ST e cambiamenti nell'onda T in quelle derivazioni che si trovano sopra la zona con ridotta afflusso di sangue (Fig. 12).
Riso. 12. ECG per angina pectoris (durante un attacco)
Le cause dell'angina pectoris sono l'ipercolesterolemia, la dislipidemia. Inoltre, l'ipertensione arteriosa, il diabete mellito, il sovraccarico psico-emotivo, la paura e l'obesità possono provocare lo sviluppo di un attacco.
A seconda di quale strato dell'ischemia del muscolo cardiaco si verifica, ci sono:
Ischemia subendocardica (sopra l'area ischemica, lo spostamento S-T è al di sotto dell'isolina, l'onda T è positiva, di grande ampiezza);
Ischemia subepicardica (elevazione del segmento S-T sopra l'isolina, T negativo).
L'insorgenza di angina pectoris è accompagnata dalla comparsa del tipico dolore dietro lo sterno, solitamente provocato dall'attività fisica. Questo dolore è di natura pressante, dura diversi minuti e scompare dopo l'uso di nitroglicerina. Se il dolore dura più di 30 minuti e non viene alleviato dall'assunzione di nitropreparati, si possono presumere con alta probabilità cambiamenti focali acuti.
Le cure di emergenza per l'angina pectoris servono ad alleviare il dolore e prevenire attacchi ricorrenti.
Vengono prescritti analgesici (da analgin a promedol), nitropreparati (nitroglicerina, sustak, nitrong, monocinque, ecc.), nonché validol e difenidramina, seduxen. Se necessario, viene eseguita l'inalazione di ossigeno.
7.2.8. infarto miocardico
L'infarto del miocardio è lo sviluppo della necrosi del muscolo cardiaco a seguito di disturbi circolatori prolungati nell'area ischemica del miocardio.
In oltre il 90% dei casi, la diagnosi viene determinata utilizzando un ECG. Inoltre, il cardiogramma consente di determinare lo stadio di un infarto, scoprirne la localizzazione e il tipo.
Un segno incondizionato di infarto è la comparsa sull'ECG di un'onda Q patologica, caratterizzata da un'ampiezza eccessiva (più di 0,03 s) e da una profondità maggiore (un terzo dell'onda R).
Le opzioni QS, QrS sono possibili. Si osservano lo spostamento S-T (Fig. 13) e l'inversione dell'onda T.
Riso. 13. ECG nell'infarto del miocardio anterolaterale (stadio acuto). Ci sono cambiamenti cicatriziali nelle parti inferiori posteriori del ventricolo sinistro
A volte c'è uno spostamento in S-T senza la presenza di un'onda Q patologica (infarto miocardico a focale piccola). Segni di un attacco di cuore:
Onda Q patologica nelle derivazioni situate sopra l'area dell'infarto;
Spostamento di un arco verso l'alto (aumento) del segmento ST rispetto all'isolina nelle derivazioni situate sopra l'area dell'infarto;
Spostamento discordante al di sotto dell'isolina del segmento ST nelle derivazioni opposte all'area dell'infarto;
Onda T negativa nelle derivazioni situate sopra l'area dell'infarto.
Con il progredire della malattia, l'ECG cambia. Questa relazione è spiegata dalla messa in scena dei cambiamenti in un attacco di cuore.
Ci sono quattro fasi nello sviluppo dell'infarto del miocardio:
Acuto;
subacuto;
Fase cicatriziale.
La fase più acuta (Fig. 14) dura diverse ore. In questo momento, il segmento ST sale bruscamente sull'ECG nelle derivazioni corrispondenti, fondendosi con l'onda T.
Riso. 14. La sequenza dei cambiamenti dell'ECG nell'infarto miocardico: 1 - Q-infarto; 2 - non Q-infarto; A - la fase più acuta; B - stadio acuto; B - stadio subacuto; D - stadio cicatriziale (cardiosclerosi post-infartuale)
Nella fase acuta si forma una zona di necrosi e compare un'onda Q anomala: l'ampiezza R diminuisce, il segmento ST rimane elevato e l'onda T diventa negativa. La durata della fase acuta è in media di circa 1-2 settimane.
Lo stadio subacuto dell'infarto dura 1-3 mesi ed è caratterizzato dall'organizzazione cicatriziale del focus della necrosi. Sull'ECG in questo momento, il segmento ST ritorna gradualmente all'isolina, l'onda Q diminuisce e l'ampiezza R, al contrario, aumenta.
L'onda T rimane negativa.
Lo stadio cicatriziale può allungarsi per diversi anni. In questo momento, si verifica l'organizzazione del tessuto cicatriziale. Sull'ECG, l'onda Q diminuisce o scompare completamente, la S-T si trova sull'isolina, la T negativa diventa gradualmente isoelettrica e quindi positiva.
Tale stadiazione è spesso indicata come la normale dinamica dell'ECG nell'infarto del miocardio.
Un infarto può essere localizzato in qualsiasi parte del cuore, ma il più delle volte si verifica nel ventricolo sinistro.
A seconda della localizzazione, si distingue l'infarto delle pareti laterali anteriori e posteriori del ventricolo sinistro. La localizzazione e la prevalenza dei cambiamenti vengono rivelate analizzando i cambiamenti dell'ECG nelle derivazioni corrispondenti (Tabella 6).
Tabella 6. Localizzazione dell'infarto del miocardio
Grandi difficoltà sorgono nella diagnosi di reinfarto, quando nuovi cambiamenti si sovrappongono a un ECG già modificato. Aiuta il controllo dinamico con la rimozione del cardiogramma a brevi intervalli.
Un tipico attacco cardiaco è caratterizzato da bruciore, forte dolore retrosternale che non scompare dopo l'assunzione di nitroglicerina.
Esistono anche forme atipiche di infarto:
Addominale (dolore al cuore e all'addome);
Asmatico (dolore cardiaco e asma cardiaco o edema polmonare);
Aritmico (dolore cardiaco e disturbi del ritmo);
Collassoide (dolore cardiaco e brusco calo della pressione sanguigna con sudorazione profusa);
Indolore.
Trattare un attacco di cuore è un compito molto difficile. Di solito è più difficile, maggiore è la prevalenza della lesione. Allo stesso tempo, secondo l'appropriata osservazione di uno dei medici zemstvo russi, a volte il trattamento di un infarto cardiaco estremamente grave procede inaspettatamente senza intoppi, e talvolta un microinfarto semplice e semplice fa firmare al medico la sua impotenza.
L'assistenza di emergenza consiste nell'arrestare il dolore (per questo vengono utilizzati narcotici e altri analgesici), eliminare anche le paure e l'eccitazione psico-emotiva con l'aiuto di sedativi, ridurre la zona infartuata (usando l'eparina) ed eliminare a loro volta altri sintomi, a seconda del grado della loro pericolosità.
Dopo il completamento del trattamento ospedaliero, i pazienti che hanno avuto un infarto vengono inviati in un sanatorio per la riabilitazione.
La fase finale è un'osservazione a lungo termine nella clinica del luogo di residenza.
7.2.9. Sindromi nei disturbi elettrolitici
Alcuni cambiamenti dell'ECG consentono di giudicare la dinamica del contenuto di elettroliti nel miocardio.
In tutta onestà, va detto che non sempre esiste una chiara correlazione tra il livello di elettroliti nel sangue e il contenuto di elettroliti nel miocardio.
Tuttavia, i disturbi elettrolitici rilevati dall'ECG servono come aiuto significativo al medico nel processo di ricerca diagnostica, nonché nella scelta del trattamento giusto.
I cambiamenti più ben studiati nell'ECG in violazione dello scambio di potassio e calcio (Fig. 15).
Riso. 15. Diagnostica ECG dei disturbi elettrolitici (A. S. Vorobyov, 2003): 1 - normale; 2 - ipokaliemia; 3 - iperkaliemia; 4 - ipocalcemia; 5 - ipercalcemia
7.2.9.1. Iperkaliemia
Segni di iperkaliemia:
Onda T a punta alta;
Accorciamento dell'intervallo Q-T;
Riducendo l'ampiezza di R.
Con grave iperkaliemia si osservano disturbi della conduzione intraventricolare.
L'iperkaliemia si verifica nel diabete (acidosi), insufficienza renale cronica, lesioni gravi con schiacciamento del tessuto muscolare, insufficienza della corteccia surrenale e altre malattie.
7.2.9.2. ipokaliemia
Segni di ipokaliemia:
Diminuzione del segmento S-T dall'alto verso il basso;
T negativo o bifase;
L'aspetto dell'U.
Con grave ipokaliemia, extrasistoli atriali e ventricolari, compaiono disturbi della conduzione intraventricolare.
L'ipopotassiemia si verifica con la perdita di sali di potassio in pazienti con vomito grave, diarrea, dopo uso prolungato di diuretici, ormoni steroidei, con una serie di malattie endocrine.
Il trattamento consiste nel reintegrare la carenza di potassio nel corpo.
7.2.9.3. Ipercalcemia
Segni di ipercalcemia:
Accorciamento dell'intervallo Q-T;
Accorciamento del segmento S-T;
Espansione del complesso ventricolare;
Disturbi del ritmo con un aumento significativo del calcio.
L'ipercalcemia si osserva con iperparatiroidismo, distruzione ossea da tumori, ipervitaminosi D e somministrazione eccessiva di sali di potassio.
7.2.9.4. ipocalcemia
Segni di ipocalcemia:
Aumento della durata dell'intervallo Q-T;
allungamento del segmento S-T;
Diminuita ampiezza di T.
L'ipocalcemia si verifica con una diminuzione della funzione delle ghiandole paratiroidi, nei pazienti con insufficienza renale cronica, con grave pancreatite e ipovitaminosi D.
7.2.9.5. Intossicazione da glicosidi
I glicosidi cardiaci sono stati a lungo utilizzati con successo nel trattamento dell'insufficienza cardiaca. Questi fondi sono indispensabili. La loro assunzione contribuisce ad una diminuzione della frequenza cardiaca (frequenza cardiaca), un'espulsione più vigorosa del sangue durante la sistole. Di conseguenza, i parametri emodinamici migliorano e le manifestazioni di insufficienza circolatoria diminuiscono.
Con un sovradosaggio di glicosidi compaiono segni caratteristici dell'ECG (Fig. 16) che, a seconda della gravità dell'intossicazione, richiedono un aggiustamento della dose o la sospensione del farmaco. I pazienti con intossicazione da glicosidi possono manifestare nausea, vomito, interruzioni nel lavoro del cuore.
Riso. 16. ECG con un sovradosaggio di glicosidi cardiaci
Segni di intossicazione da glicosidi:
Diminuzione della frequenza cardiaca;
Accorciamento della sistole elettrica;
Diminuzione del segmento S-T dall'alto verso il basso;
Onda T negativa;
Extrasistoli ventricolari.
L'intossicazione grave con glicosidi richiede l'interruzione del farmaco e la nomina di preparazioni di potassio, lidocaina e beta-bloccanti.